摘要:[教后小结] 第二课时 维生素 [你知道什么?]你知道哪些食品中富含维生素?缺乏维生素可引起什么疾病? [教师讲述]维生素 维 生 素 来源 水果.蔬菜.糙米.面包-- 类别 及作 用 VA--促进正常发育.增强抵抗力.防止视力下降 VB--维持正常的新陈代谢和神经系统的正常生理功能.防止神经炎.消化不良.口腔溃疡等 VC--维持骨骼.肌肉和血管的正常生理作用.增强抵抗力.防止牙龈出血.感冒等 VD--促进钙.磷吸收和骨骼发育.防止骨质疏松.骨折等 VE--抗衰老.防止腿抽筋等 [练习]课后225页 [作业]每课三练 [板书]维生素1. 来源:水果.蔬菜.糙米.面包--
网址:http://m.1010jiajiao.com/timu3_id_145005[举报]
 金属镁将成为二十一世纪大有前途的绿色金属材料.
金属镁将成为二十一世纪大有前途的绿色金属材料.
海水中的MgCl2熟石灰过滤Mg(OH)2蒸发、浓缩、结晶MgCl2?6H2O脱水MgCl2通电Mg
(1)占地球表面积70%的海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
①在实验室进行过滤操作时需要用到玻璃棒,其作用是______.
②电解熔融氯化镁的过程中,______能转化为______能.
③写出氯化镁与熟石灰反应的化学方程式______.
(2)①取两块大小相同的干冰,在干冰中央挖一个小穴,撒入一些镁粉,用红热的铁棒把镁点燃,将另一块干冰盖上,你会看到镁粉在干冰内继续燃烧,发出耀眼的白光,像冰灯一样.已知该反应的生成物是氧化镁和碳.此反应的方程式是______,此反应属于______反应(判断基本反应类型).该实验证明干冰具有______的性质(答一条即可);为验证上述反应所得固体中无剩余镁,可向该固体中加入试剂得名称为______,反应的现象是______.②金属镁在高温下与氮气反应生成氮化镁,氮化镁中氮元素的化合价-3.据此写出氮化镁的化学式______.
(3)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色,这层灰黑色是什么物质呢?
猜想:小明认为可能是MgO;小赵认为可能是Mg2(OH)2CO3;小花认为可能是Mg(OH)2.小赵认为小明的猜想是错误的,其理由是______.
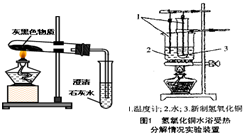
实验探究:小赵按右图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.实验分析:实验后,小赵认为小花的猜测也是错误的,其理由______.
查阅资料得出结论:Mg(OH)2和Mg2(OH)2CO3都可以加热分解,产物均为氧化物,请写出Mg2(OH)2CO3加热分解的化学方程式_____________..
(4)镁铝合金广泛用于火箭、导弹和飞机制造业等.某兴趣小组为探究镁铝合金的组成,取16g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中(只有铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,镁与氢氧化钠溶液不反应),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | 5.2 | 4.0 |
今天又是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他分
别取两种少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
| 猜想与假设 | 实验步骤 | 现象及结论 |
| 此气体可能是氧气 | 收集产生的气体,________ | ________. |
Ⅱ.(1)老师所拿试管中产生氧气的文字表达式可能是________.

(2)利用老师提供的固体和液体试剂制取该气体,采用的发生装置可选取图1中的________(填序号).
(3)图2是排空气法收集该气体的装置,气体由________端(填“a”或“b”)导入.若使用排水法,水由________端(填“a”或“b”)排出.
III.除了老师提供的固体和液体药品混合可以制取氧气,我还知道其它途径可制取氧气.小明同学对目前学过的可以制取氧气的方法进行了如下的小结:
A.加热氧化汞
B.分离空气
C.________
D.加热分解高锰酸钾
E.分解过氧化氢
(1)请你在C处再写出一种制取氧气的方法.
(2)请写出实验室用高锰酸钾制取氧气的文字表达式:________.
(3)若选用Ⅱ中A装置利用加热分解高锰酸钾制取氧气,实验完毕,停止加热前应该________
A.先撤导管出水,后熄灭酒精灯 B.先熄灭酒精灯,后撤导管出水. 查看习题详情和答案>>
某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数.取25g石灰石样品(假设杂质既不溶于水,也不与其他物质反应)放入烧杯中,向其中分五次加入一定溶质质量分数的稀盐酸,每次加入50g稀盐酸.每次加入稀盐酸后烧杯中剩余质量如下表所示:
| 相关的质量 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 所加入稀盐酸的质量(g) | 50 | 50 | 50 | 50 | 50 |
| 烧杯中剩余的质量(g) | 72.8 | 120.6 | 168.4 | 216.2 | 266.2 |
(1)写出反应的化学方程式:______
(2)列出求解该样品中参加反应的碳酸钙质量(x)的比例式______;
(3)该样品中碳酸钙的质量分数为______;
(4)将前四次实验过滤,得到只含一种溶质的不饱和溶液,若想使所得溶液的溶质的质量分数为10%,则需要向此溶液中加入水______g;
(5)若要制取含杂质1 6%的生石灰1 00t,需上述石灰石______. (假设制取过程中石灰石的利用率为75%) 查看习题详情和答案>>
2010年5月12日,在苍茫海水中沉没了800多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑.已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.
实验用到的主要装置为:

(1)装置连接顺序为:________.(填写编号)
(2)操作步骤及数据处理:
第一步 检查气密性;
第二步 装入药品,称取装置①和③的质量;
第三步 试验后再次称取装置①和③的质量,记录数据如表;
质 装置 量 时间 | 装置① | 装置③ |
| 实验前 | 220.0克 | 195.0克 |
| 实验后 | 222.1克 | 199.4克 |
(3)结果分析;从下列选项中选出产生该实验结果可能的原因有哪些?________.
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解. 查看习题详情和答案>>