网址:http://m.1010jiajiao.com/timu3_id_141738[举报]
表一:硫酸的密度和溶质质量分数对照表(20℃)


(1)由表一可得出的规律是: _________ .
(2)由表二可得出两种物质溶解度差异的规律是: _________ .
(3)我国有许多盐碱湖,湖水中溶有大量的氯化钠和碳酸钠,那里的农民“冬天捞碱、夏天晒盐”.试说明其中的道理: _________ .
表一:硫酸的密度和溶质质量分数对照表(20 ℃)


(1)由表一可得出的规律是:________________________________________________。
(2)由表二可得出两种物质溶解度差异的规律是:____________________________________。
(3)我国有许多盐碱湖,湖水中溶有大量的氯化钠和碳酸钠,那里的农民“冬天捞碱、夏天晒盐”。试说明其中的道理:__________________________________________________________。
地球上物质种类千差万别,但都有一定的规律可寻:
表一:硫酸的密度和溶质质量分数对照表(20 ℃)
| 密度/g·cm-3) | 1.01 | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
| 溶质质量分数/% | 1 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 98 |
表二:氯化钠和碳酸钠晶体的溶解度对照表(0 ℃—30 ℃)
| 温度/℃ 物质 | 0 | 10 | 20 | 30 |
| 氯化钠 | 35.7 g | 35.8 g | 36 g | 36.3 g |
| 碳酸钠晶体 | 7 g | 12.5 g | 21.5 g | 38.8 g |
请你分析上述两个表中的内容,并探究下列问题:
(1)由表一可得出的规律是:________________________________________________。
(2)由表二可得出两种物质溶解度差异的规律是:____________________________________。
(3)我国有许多盐碱湖,湖水中溶有大量的氯化钠和碳酸钠,那里的农民“冬天捞碱、夏天晒盐”。试说明其中的道理:__________________________________________________________。
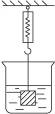
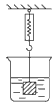
(4)如图,烧杯内盛有不饱和氯化钠溶液,弹簧秤上挂了一块与氯化钠不反应且不溶解的金属块。向氯化钠溶液中加适量氯化钠晶体,则弹簧秤的示数将(填“变大”“变小”或“不变”)____________。
查看习题详情和答案>>地球上物质种类千差万别,但都有一定的规律可寻:
表一:硫酸的密度和溶质质量分数对照表(20 ℃)
| 密度/g·cm-3) | 1.01 | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
| 溶质质量分数/% | 1 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 98 |
表二:氯化钠和碳酸钠晶体的溶解度对照表(0 ℃—30 ℃)
| 温度/℃ 物质 | 0 | 10 | 20 | 30 |
| 氯化钠 | 35.7 g | 35.8 g | 36 g | 36.3 g |
| 碳酸钠晶体 | 7 g | 12.5 g | 21.5 g | 38.8 g |
请你分析上述两个表中的内容,并探究下列问题:
(1)由表一可得出的规律是:________________________________________________。
(2)由表二可得出两种物质溶解度差异的规律是:____________________________________。
(3)我国有许多盐碱湖,湖水中溶有大量的氯化钠和碳酸钠,那里的农民“冬天捞碱、夏天晒盐”。试说明其中的道理:__________________________________________________________。

(4)如图,烧杯内盛有不饱和氯化钠溶液,弹簧秤上挂了一块与氯化钠不反应且不溶解的金属块。向氯化钠溶液中加适量氯化钠晶体,则弹簧秤的示数将(填“变大”“变小”或“不变”)____________。
查看习题详情和答案>>地球上物质种类千差万别,但都有一定的规律可寻:
表一:硫酸的密度和溶质质量分数对照表(20 ℃)
| 密度/g·cm-3) | 1.01 | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.81 | 1.84 |
| 溶质质量分数/% | 1 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 98 |
表二:氯化钠和碳酸钠晶体的溶解度对照表(0 ℃—30 ℃)
| 温度/℃ 物质 | 0 | 10 | 20 | 30 |
| 氯化钠 | 35.7 g | 35.8 g | 36 g | 36.3 g |
| 碳酸钠晶体 | 7 g | 12.5 g | 21.5 g | 38.8 g |
请你分析上述两个表中的内容,并探究下列问题:
(1)由表一可得出的规律是:________________________________________________。
(2)由表二可得出两种物质溶解度差异的规律是:____________________________________。
(3)我国有许多盐碱湖,湖水中溶有大量的氯化钠和碳酸钠,那里的农民“冬天捞碱、夏天晒盐”。试说明其中的道理:_________________________________________________________。

(4)如图,烧杯内盛有不饱和氯化钠溶液,弹簧秤上挂了一块与氯化钠不反应且不溶解的金属块。向氯化钠溶液中加适量氯化钠晶体,则弹簧秤的示数将(填“变大”“变小”或“不变”)____________。
查看习题详情和答案>>