摘要:25.6.质量守恒
网址:http://m.1010jiajiao.com/timu3_id_139807[举报]
质量守恒定律是重要的三大定律之一,应用它可以帮助我们解决许多生产、科学实验和生活上的问题.现有氯酸钾和二氧化锰的混合物共26.5g,加热使之反应,待反应至不再有气体生成后,将试管冷却、称量,得到剩余固体16.9g.求:
(1)制取氧气的质量共为
(2)原混合物中氯酸钾多少克?(写出解题过程)
查看习题详情和答案>>
(1)制取氧气的质量共为
9.6
9.6
g.(2分);(2)原混合物中氯酸钾多少克?(写出解题过程)
质量守恒定律的定量研究对化学科学发展具有重大作用.
(1)黑火药点燃时发生如下反应:2KNO3+S+3C
K2S+3CO2↑+X↑,其中X的化学式为
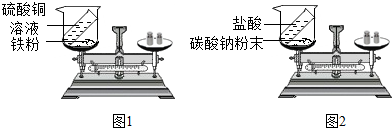
(2)如图1装置中,称量小烧杯及烧杯内所有物质的总质量为m1,然后将小烧杯中的硫酸铜溶液和铁粉完全混合,反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为 m2,则(填“=”“>”“<”)m1
(3)如图2装置中,称量小烧杯及烧杯内所有物质的总质量为m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为 m2,则(填“=”“>”“<”)m1
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质的总质量
(5)在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的认识不正确的是
A.物质Y可能是该反应的催化剂 B.该反应的基本类型为分解反应
C.参加反应的Z与 W的质量比为2:3 D.反应后容器中Z与Y的质量比为6:1.
查看习题详情和答案>>

(1)黑火药点燃时发生如下反应:2KNO3+S+3C
| 点燃 |
N2
N2
.(2)如图1装置中,称量小烧杯及烧杯内所有物质的总质量为m1,然后将小烧杯中的硫酸铜溶液和铁粉完全混合,反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为 m2,则(填“=”“>”“<”)m1
=
=
m2.(3)如图2装置中,称量小烧杯及烧杯内所有物质的总质量为m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发生了一段时间后,再称量小烧杯及烧杯内物质的总质量为 m2,则(填“=”“>”“<”)m1
>
>
m2,其原因为因生成的二氧化碳扩散到空气中,依据质量守恒定律,反应前烧杯中反应物的总质量大于使反应后烧杯中剩余物的总质量.
因生成的二氧化碳扩散到空气中,依据质量守恒定律,反应前烧杯中反应物的总质量大于使反应后烧杯中剩余物的总质量.
(4)由此可知,在化学反应前后,一定不变的是①②⑤⑥
①②⑤⑥
(填序号).①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质的总质量
(5)在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的认识不正确的是
B、C
B、C
| 物 质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 17 | m | 6 | 11 |
C.参加反应的Z与 W的质量比为2:3 D.反应后容器中Z与Y的质量比为6:1.
质量守恒定律的定量研究对化学科学的发展具有重大意义.

(1)甲、乙、丙三个小组的同学按照如图1所示的实验探究质量守恒定律.实验中,三个小组的同学得到下列数据,其中不合理的数据是 (填组别),不合理的理由是 .
(2)如图2为某化学反应的微观示意图:
①反应中,以下叙述正确的是 .
A.原子的种类没有改变
B.原子的个数没有改变
C.分子的个数没有改变
②该反应的化学方程式为 .
(3)在化学反应A+B═C+D中,若12gA与一定量的B恰好完全反应,生成28gC和2gD,则参加反应的A与B的质量比为 .
查看习题详情和答案>>

(1)甲、乙、丙三个小组的同学按照如图1所示的实验探究质量守恒定律.实验中,三个小组的同学得到下列数据,其中不合理的数据是
| 反应前后质量组别 | 甲组 | 乙组 | 丙组 |
| 盐酸与碳酸钠粉末反应前称量(g) | 85.3 | 82.8 | 86.5 |
| 盐酸与碳酸钠粉末反应后称量(g) | 85.3 | 80.6 | 87.8 |
①反应中,以下叙述正确的是
A.原子的种类没有改变
B.原子的个数没有改变
C.分子的个数没有改变
②该反应的化学方程式为
(3)在化学反应A+B═C+D中,若12gA与一定量的B恰好完全反应,生成28gC和2gD,则参加反应的A与B的质量比为
质量守恒定律是一条重要规律.请利用该规律的相关知识回答下列问题.
(1)蜡烛在空气中燃烧时生成二氧化碳和水.由此判断蜡烛中一定含有的元素是 (填元素符号),判断的依据是 .
(2)某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热并冷却后再次称量,其质量为m2 g,则m1 m2 (填“>”、“<”或“=”),产生这一结果的原因是 .
(3)在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表.关于此反应的认识正确的是 (填字母序号).
A.m=1
B.该反应为分解反应
C.X与Z的化学计量数之比是3:2
D.若该反应充分进行,反应后W仍有剩余.
查看习题详情和答案>>
(1)蜡烛在空气中燃烧时生成二氧化碳和水.由此判断蜡烛中一定含有的元素是
(2)某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热并冷却后再次称量,其质量为m2 g,则m1
(3)在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表.关于此反应的认识正确的是
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 一段时间后的质量(g) | 17 | m | 6 | 11 |
B.该反应为分解反应
C.X与Z的化学计量数之比是3:2
D.若该反应充分进行,反应后W仍有剩余.
质量守恒定律是一条重要规律。请利用该规律的相关知识回答下列问题。
(1)蜡烛在空气中燃烧时生成二氧化碳和水。由此判断蜡烛中一定含有的元素是
(填元素符号),判断的依据是 。
(2)某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热并冷却后再次称量,其质量为m2 g,则m1 m2 (填“>”、“<”或“=”),产生这一结果的原因是 。
(3)在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表。关于此反应的认识正确的是 (填字母序号)。
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 一段时间后的质量(g) | 17 | m | 6 | 11 |
A.m = 1
B.该反应为分解反应
C.X与Z的化学计量数之比是3:2
D.若该反应充分进行,反应后W仍有剩余
查看习题详情和答案>>