摘要:氨气(NH3)是一种无色.有刺激性气味的气体.极易溶于水.它的水溶液称为氨水.显碱性.氨在化学工业中用途很广泛.例如制化肥.制纯碱等,近年来.氨还用于环境治理. ⑴实验室收集氨气可采用的方法为 .干燥氨气可选用试剂为 . ⑵工业上在细菌作用下用氨处理含甲醇的废水.使其变为毒的N2和CO2.从而消除对环境的污染.有关的反应为:6NH3+5CH3OH+123N2+5CO2+19H2O.上述反应中B的化学式是 . ⑶在400℃.催化剂存在的条件下.用氨气可将有毒气体NO还原.生成N2和H2O. 试写出该反应的化学方程式: .
网址:http://m.1010jiajiao.com/timu3_id_138163[举报]
氨气(NH3)是一种无色、有刺激性气味的气体,极易溶于水,它的水溶液称为氨水,显碱性。氨在化学工业中用途很广泛,例如制化肥、制纯碱等;近年来,氨还用于环境治理。
(1)工业上在细菌的作用下用氨处理含甲醇的废水,使其变为无毒的氮气和二氧化碳,从而消除对环境的污染,有关的反应是:6NH3+5CH3OH+12B![]() 3N2+5CO2+19H2O,上述反应中B的化学式____________;细菌的作用是______________________;叫________剂。
3N2+5CO2+19H2O,上述反应中B的化学式____________;细菌的作用是______________________;叫________剂。
(2)在400℃、催化剂存在的条件下,用氨气可将有毒气体一氧化氮还原,生成氮气和水,试写出该反应的化学方程式:____________________________
查看习题详情和答案>>
氨气(NH3)是一种无色、有刺激性气味的气体,极易溶于水,它的水溶液称为氨水,呈碱性.氨气在化学工业中用途很广泛,例如制化肥、制纯碱等,近几年来,氨还用于环境治理.
(1)氨分子中氮、氢元素的质量比为________.
(2)“侯氏制碱法”关键一步反应的原理可表示为:NH3+CO2+H2O+NaCl![]() NaHCO3+A其中生成物A也可用作化肥,A中氮元素的质量分数为________.
NaHCO3+A其中生成物A也可用作化肥,A中氮元素的质量分数为________.
(3)在细菌作用下,用氨处理含甲醇的工业废水,使其变为无毒的N2和CO2,从而清除对环境的污染,有关反应的化学方程式为:
上述反应中B的化学式是________.
(4)在400℃左右、有催化剂存在的条件下,用氨气可将有毒气体NO还原为N2和H2O,试写出该反应的化学方程式:________.
氨气
(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水.回答下列问题:(1)实验室制取氨气的化学方程式为:________;最好选用下图________(选填装置A、B、C、D)气体发生装置制取氨气.
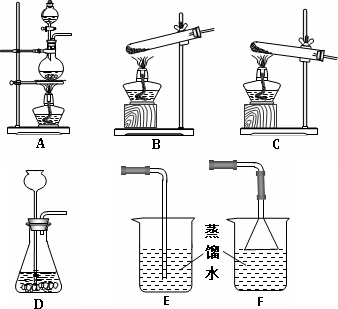
(2)欲制得氨气(氨气溶于水),且能避免倒吸,最好在其发生装置后连接下图________装置.(选填E或F).