摘要:19.某想用废铜米制得硫酸铜溶液.实验过程如下: (1)将废铜在空气中加热.有关反应的化学方程式是 , (2)实验过程中加入稀硫酸.有关反应的化学方程式是 , (3)过滤操作时用到的仪器有:玻璃棒.烧杯.漏斗. .
网址:http://m.1010jiajiao.com/timu3_id_133226[举报]
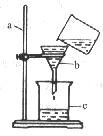 9、如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.
9、如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.试回答:
(1)写出标号仪器的名称:
a
铁架台.
,b
漏斗.
,c
烧杯.
.(2)该图中存在的三处明显错误是:
①
未用玻璃棒引流.
;②
滤纸边缘高于漏斗边缘.
;③
漏斗径尖端部分未靠在烧杯内壁上.
;(3)操作过程中,他发现过滤速度太慢,产生的原因可能是
滤纸没有紧贴漏斗内壁(或滤纸与漏斗之间留有气泡)
;(4)过滤后观察发现,滤液仍然浑浊,可能的原因是
滤纸破损,液面高于滤纸边缘.
(要求写两条).(5)该同学将过滤装置进行了改进,改进后过滤,得到了澄清透明的水,他兴奋的宣布:我终于制得了纯水!对此你有无不同看法?理由是
不是纯水,因过滤后的水还含可溶性杂质.
;若要制得纯水,还需采用的净化方法是
蒸馏.
.
实验是进行科学探究的重要途径,在探究过程中,很多因素都会对实验结果产生影响.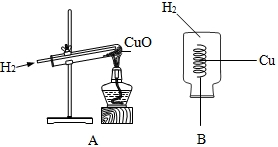
(1)反应物的浓度不同,反应现象不同.请举出实例说明.
(2)碳在充足的氧气中燃烧生成二氧化碳,在不足的氧气中燃烧生成一氧化碳.对比这两个反应可以得到的结论是 .
(3)H2在加热条件下可以与CuO反应,生成Cu和H2O.
①亮亮同学利用图A装置完成了该实验.
实验步骤:先通入H2,再加热,实验结束后,先撤酒精灯,继续通入H2直至试管冷却.可观察到黑色CuO变成红色.
②明明同学利用图B装置也完成了该实验.实验步骤:将铜丝在酒精灯外焰上加热变黑后,迅速伸入盛有H2的集气瓶中,片刻可观察到黑色CuO变为红色.
对比A、B两套装置,B装置的优点是 .
③在明明同学的实验中,当铜丝表明生成CuO后,若继续在酒精灯外焰上加热至炽热状态时,则与H2反应较快;若只加热至红热状态时,则反应较慢,甚至没有明现现象.对比这两种情况,可得到的结论是 .
(4)在用废铜屑制取硫酸铜的实验中,有下列两种方案可供选择:
甲方案:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
乙方案:2CuO+O2
2CuO,CuO+H2SO4═CuSO4+2H2O
①分别用上述两种方案制取80g硫酸铜,甲方案参加反应的硫酸的质量为98g,请计算乙方案中参加反应的硫酸的质量为多少?
②通过对比这两种实验方案及计算结果,你认为选用哪种方案更好? ;请说明你的理由 .
(5)通过对上述实验的对比与分析可知,探究某一化学问题时,除了应根据具体情况考虑恰当的实验装置外,还应考虑 等因素.
查看习题详情和答案>>

(1)反应物的浓度不同,反应现象不同.请举出实例说明.
(2)碳在充足的氧气中燃烧生成二氧化碳,在不足的氧气中燃烧生成一氧化碳.对比这两个反应可以得到的结论是
(3)H2在加热条件下可以与CuO反应,生成Cu和H2O.
①亮亮同学利用图A装置完成了该实验.
实验步骤:先通入H2,再加热,实验结束后,先撤酒精灯,继续通入H2直至试管冷却.可观察到黑色CuO变成红色.
②明明同学利用图B装置也完成了该实验.实验步骤:将铜丝在酒精灯外焰上加热变黑后,迅速伸入盛有H2的集气瓶中,片刻可观察到黑色CuO变为红色.
对比A、B两套装置,B装置的优点是
③在明明同学的实验中,当铜丝表明生成CuO后,若继续在酒精灯外焰上加热至炽热状态时,则与H2反应较快;若只加热至红热状态时,则反应较慢,甚至没有明现现象.对比这两种情况,可得到的结论是
(4)在用废铜屑制取硫酸铜的实验中,有下列两种方案可供选择:
甲方案:Cu+2H2SO4(浓)
| ||
乙方案:2CuO+O2
| ||
①分别用上述两种方案制取80g硫酸铜,甲方案参加反应的硫酸的质量为98g,请计算乙方案中参加反应的硫酸的质量为多少?
②通过对比这两种实验方案及计算结果,你认为选用哪种方案更好?
(5)通过对上述实验的对比与分析可知,探究某一化学问题时,除了应根据具体情况考虑恰当的实验装置外,还应考虑
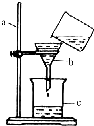 水是生命之源,它的保护和合理利用已受到人们的普遍关注.
水是生命之源,它的保护和合理利用已受到人们的普遍关注.(1)请你说出“保护水资源,刻不容缓”的两点理由:
①
淡水资源有限
淡水资源有限
;②水资源正在不断受到严重的污染
水资源正在不断受到严重的污染
.(2)结合你的日常生活实际,谈谈你能做到的保护水资源两点做法:
①
节约用水
节约用水
;②防止水体污染
防止水体污染
.(3)右图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.
①写出标号仪器的名称:a
铁架台
铁架台
,b漏斗
漏斗
,c烧杯
烧杯
.②该图中存在的两处明显错误A
未用玻璃棒引流
未用玻璃棒引流
B漏斗下端管口未靠烧杯内壁
漏斗下端管口未靠烧杯内壁
. 改正错误之处后,该同学经过过滤得到的净水是混合物
混合物
(填“纯净物”或“混合物”),原因是水中还有很多可溶性物质存在
水中还有很多可溶性物质存在
;若经过两次过滤后滤液仍然浑浊,其原因可能滤纸破损(液面超过滤纸边缘)
滤纸破损(液面超过滤纸边缘)
(写一条即可).(4)使用硬水会给生活和生产带来许多麻烦,试举一例说明
锅炉爆炸
锅炉爆炸
.在日常生活中,人们常用煮沸
煮沸
的方法来降低水的硬度.如果想知道得到的水是软水还是硬水,我们可以用肥皂水
肥皂水
来检验.
实验是进行科学探究的重要途径,在探究过程中,很多因素都会对实验结果产生影响.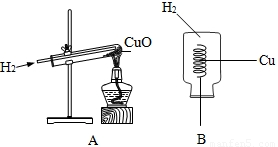
(1)反应物的浓度不同,反应现象不同.请举出实例说明.
______
(2)碳在充足的氧气中燃烧生成二氧化碳,在不足的氧气中燃烧生成一氧化碳.对比这两个反应可以得到的结论是______.
(3)H2在加热条件下可以与CuO反应,生成Cu和H2O.
①亮亮同学利用图A装置完成了该实验.
实验步骤:先通入H2,再加热,实验结束后,先撤酒精灯,继续通入H2直至试管冷却.可观察到黑色CuO变成红色.
②明明同学利用图B装置也完成了该实验.实验步骤:将铜丝在酒精灯外焰上加热变黑后,迅速伸入盛有H2的集气瓶中,片刻可观察到黑色CuO变为红色.
对比A、B两套装置,B装置的优点是______.
③在明明同学的实验中,当铜丝表明生成CuO后,若继续在酒精灯外焰上加热至炽热状态时,则与H2反应较快;若只加热至红热状态时,则反应较慢,甚至没有明现现象.对比这两种情况,可得到的结论是______.
(4)在用废铜屑制取硫酸铜的实验中,有下列两种方案可供选择:
甲方案:Cu+2H2SO4(浓)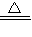 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
乙方案:2CuO+O2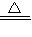 2CuO,CuO+H2SO4═CuSO4+2H2O
2CuO,CuO+H2SO4═CuSO4+2H2O
①分别用上述两种方案制取80g硫酸铜,甲方案参加反应的硫酸的质量为98g,请计算乙方案中参加反应的硫酸的质量为多少?
______
②通过对比这两种实验方案及计算结果,你认为选用哪种方案更好?______;请说明你的理由______.
(5)通过对上述实验的对比与分析可知,探究某一化学问题时,除了应根据具体情况考虑恰当的实验装置外,还应考虑______等因素.
查看习题详情和答案>>

(1)反应物的浓度不同,反应现象不同.请举出实例说明.
______
(2)碳在充足的氧气中燃烧生成二氧化碳,在不足的氧气中燃烧生成一氧化碳.对比这两个反应可以得到的结论是______.
(3)H2在加热条件下可以与CuO反应,生成Cu和H2O.
①亮亮同学利用图A装置完成了该实验.
实验步骤:先通入H2,再加热,实验结束后,先撤酒精灯,继续通入H2直至试管冷却.可观察到黑色CuO变成红色.
②明明同学利用图B装置也完成了该实验.实验步骤:将铜丝在酒精灯外焰上加热变黑后,迅速伸入盛有H2的集气瓶中,片刻可观察到黑色CuO变为红色.
对比A、B两套装置,B装置的优点是______.
③在明明同学的实验中,当铜丝表明生成CuO后,若继续在酒精灯外焰上加热至炽热状态时,则与H2反应较快;若只加热至红热状态时,则反应较慢,甚至没有明现现象.对比这两种情况,可得到的结论是______.
(4)在用废铜屑制取硫酸铜的实验中,有下列两种方案可供选择:
甲方案:Cu+2H2SO4(浓)
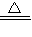 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O乙方案:2CuO+O2
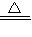 2CuO,CuO+H2SO4═CuSO4+2H2O
2CuO,CuO+H2SO4═CuSO4+2H2O①分别用上述两种方案制取80g硫酸铜,甲方案参加反应的硫酸的质量为98g,请计算乙方案中参加反应的硫酸的质量为多少?
______
②通过对比这两种实验方案及计算结果,你认为选用哪种方案更好?______;请说明你的理由______.
(5)通过对上述实验的对比与分析可知,探究某一化学问题时,除了应根据具体情况考虑恰当的实验装置外,还应考虑______等因素.
查看习题详情和答案>>
如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图。
试回答:
(1)该图中存在的三处明显错误是:
①_____________________________________________;
②_____________________________________________;
③_____________________________________________。
(2)操作过程中,他发现过滤速度太慢,产生的原因可能是_____________________________________________ ;
(3)过滤后观察发现,滤液仍然浑浊,可能的原因是______________________________________________(写出一点即可)。
(4)该同学将过滤装置进行了改进,改进后过滤,得到了澄清透明的水,他兴奋的宣布:我终于制得了纯水!对此你有无不同看法?理由是__________________________________________ ____;若要制得纯水,还需采用的净化方法是___________。
将燃烧的木条放在集气瓶口,观察木条是否熄灭
查看习题详情和答案>>