摘要:向密闭的容器中通入氧气和一氧化氮气体.已知:2NO+O2====2NO2.则最终容器内氧原子和氮原子个数之比为( ) A.2(a+b)/b ?B.2a/b? C./b ? D.b/a? 思路解析:此题为质量守恒定律的运用题.质量守恒定律不仅体现在宏观上总质量相等.元素的质量相等.还体现在微观上原子个数相等.NO和O2发生反应.反应前后氮原子和氧原子个数保持不变.即氮原子数为b个.氧原子数为个. 答案:C
网址:http://m.1010jiajiao.com/timu3_id_132065[举报]
向密闭的容器中通入氧气(含a个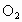 分子)和一氧化氮(含b个NO分子)气体,已知:
分子)和一氧化氮(含b个NO分子)气体,已知: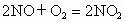 ,则最终容器内氧原子和氮原子个数之比为
,则最终容器内氧原子和氮原子个数之比为
[
]|
A .2(a+b)/b |
B .2a/b |
|
C .(2a+b)/b |
D .b/a |
向密闭的容器中通入氧气(含a个 分子)和一氧化氮(含b个NO分子)气体,已知:
分子)和一氧化氮(含b个NO分子)气体,已知: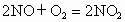 ,则最终容器内氧原子和氮原子个数之比为
,则最终容器内氧原子和氮原子个数之比为
[
]|
A .2(a+b)/b |
B .2a/b |
|
C .(2a+b)/b |
D .b/a |