摘要:用A.B两个烧杯各取90克溶质的质量分数为10%的硝酸钾溶液.再向A烧杯中加入10 g硝酸钾.向B烧杯中加入10 g水.并用玻璃棒搅拌至全部溶解. [讨论] (1)原溶液中溶质的质量是多少?溶液的质量是多少?溶剂的质量是多少? (2)向原溶液中增加10克硝酸钾或增加10克水后.溶液中溶质质量.溶剂质量.溶液质量各是多少? 思路解析:(1)溶液的质量=90克 溶质的质量=溶液质量×溶质的质量分数 =90克×10%=9克 溶剂的质量=溶液质量-溶质质量 =90克-9克=81克 (2)①增加10克硝酸钾后: 溶质质量=9克+10克=19克 溶剂质量=81克 溶液质量=19克+81克=100克 或90克+10克=100克 则可知:(1)增加10克溶质后: 溶质的质量分数=×100% =×100%=19% 注:若新增的10克溶质未完全溶解.则上述计算错误. ②加入10克水后: 溶质质量=9克 溶剂质量=81克+10克=91克 溶液质量=9克+91克=100克 或90克+10克=100克 则可知:增加10克水后: 溶质的质量分数=×100% =×100%=9% 答案:(1)9 g 90 g 81 g (2)①加10 g KNO3时.19 g.81 g.100 g ②加10 g H2O时.9 g.91 g.100 g
网址:http://m.1010jiajiao.com/timu3_id_131941[举报]
 如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.过一段时间看到的现象是
如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.过一段时间看到的现象是A烧杯中液体变红
A烧杯中液体变红
,该实验说明分子是不断运动的
分子是不断运动的
.一些同学对上述结论有不同看法,主要有以下两种猜测:
第一种:B烧杯中的蒸馏水使酚酞试液变红
第二种:B烧杯中浓氨水挥发出氨气,扩散到A烧杯中的溶液中使酚酞试液变红.
①你认为
第二种
第二种
猜测正确.②为证明这两种猜测,现设计如下的实验(请完成下表)
| 实验内容、方法 | 现象 | 结论 |
| 用洁净的小烧杯取20mL水,滴入2-3滴酚酞试液,观察现象 | 不变色 | 水 不能 不能 使酚酞变色(填“能”或“不能”,下同. |
| 取一张滤纸,滴入酚酞试液,待晾干后,放在装上有浓氨水的试剂瓶上方. | 酚酞不变色 | 氨气 不能 不能 使酚酞变色. |
| 将少量氨气通入含有酚酞试液的蒸馏水中 | 溶液变成 红 红 色 |
氨气溶解在水中形成的氨水能使酚酞变色 |
在小烧杯A中加入20mL蒸馏水,滴入2~3滴紫色石蕊试液,得到的溶液呈紫色.小烧杯B中加入20mL浓盐酸(盐酸是氯化氢气体溶于水形成的溶液);用一只大烧杯把A、B两个烧杯罩在一起(如图).过几分钟,看到烧杯A中的溶液变成了红色.
(1)你认为溶液变红的原因可能有哪些?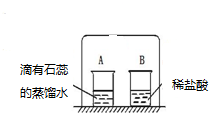
假设1:
假设2:
(2)请设计简单的实验证明你的假设1.
(3)通过实验获取的最后结论:
查看习题详情和答案>>
(1)你认为溶液变红的原因可能有哪些?

假设1:
浓盐酸易挥发,挥发出的氯化氢气体溶解在水中使石蕊试液变红
浓盐酸易挥发,挥发出的氯化氢气体溶解在水中使石蕊试液变红
假设2:
空气使石蕊试液变红
空气使石蕊试液变红
(2)请设计简单的实验证明你的假设1.
| 操作方法 | 实验现象 | 结论 | |
| 验证假设1的实验 | 向浓盐酸中滴加几滴石蕊试液 向浓盐酸中滴加几滴石蕊试液 |
石蕊试液变红 石蕊试液变红 |
浓盐酸易挥发,挥发出的氯化氢气体溶解在水中使石蕊试液变红 浓盐酸易挥发,挥发出的氯化氢气体溶解在水中使石蕊试液变红 |
浓盐酸有挥发性,挥发出的氯化氢气体溶解在水中使石蕊试液变红
浓盐酸有挥发性,挥发出的氯化氢气体溶解在水中使石蕊试液变红
. 在小烧杯A中加入20mL蒸馏水,滴入2~3滴紫色石蕊试液,得到的溶液呈紫色.在小烧杯B中加入20mL浓盐酸(盐酸是氯化氢气体溶于水形成的溶液);用一只大烧杯把A、B两个烧杯罩在一起(如图所示).过几分钟,看到烧杯A中的溶液变成红色.
在小烧杯A中加入20mL蒸馏水,滴入2~3滴紫色石蕊试液,得到的溶液呈紫色.在小烧杯B中加入20mL浓盐酸(盐酸是氯化氢气体溶于水形成的溶液);用一只大烧杯把A、B两个烧杯罩在一起(如图所示).过几分钟,看到烧杯A中的溶液变成红色.(1)你认为烧杯A中的溶液变红的原因可能有哪些?
假设1:
空气使石蕊试液变红
空气使石蕊试液变红
;假设2:
浓盐酸易挥发,挥发出的氯化氢气体溶解在水中使石蕊试液变红
浓盐酸易挥发,挥发出的氯化氢气体溶解在水中使石蕊试液变红
.(2)请设计简单的实验,探究你的假设(简述操作方法):
验证假设1的实验:
将滴有石蕊试液的蒸馏水暴露在空气中观察其颜色是否改变
将滴有石蕊试液的蒸馏水暴露在空气中观察其颜色是否改变
;验证假设2的实验:
向浓盐酸中滴加几滴石蕊试液观察其颜色是否改变
向浓盐酸中滴加几滴石蕊试液观察其颜色是否改变
.(3)通过实验探究,获得的结论是
浓盐酸有挥发性,挥发出的氯化氢气体溶解在水中使石蕊试液变红
浓盐酸有挥发性,挥发出的氯化氢气体溶解在水中使石蕊试液变红
.已知酸性物质可使紫色的石蕊试液变成红色,某同学为了探究微粒的一些性质,设计了如下的系列实验:

(1)向一小烧杯中加入蒸馏水,然后滴加紫色石蕊试液(如图Ⅰ),观察到的实验现象是烧杯里的水变成了
(2)向(Ⅰ)中的烧杯中再加入稀盐酸,观察到的实验是紫色石蕊试液变成
(3)分别取A、B两个烧杯,A杯中加入蒸馏水,再向其中加入紫色石蕊,B杯中盛有浓盐酸,用一大烧杯把A、B两烧杯的溶液罩在一起(如图Ⅱ),过一段时间后观察到的现象是A烧杯中的紫色石蕊试液变
(4)上述实验还说明浓盐酸的两个重要的性质分别是:
①物理性质:浓盐酸具有
②化学性质:浓盐酸具有
查看习题详情和答案>>

(1)向一小烧杯中加入蒸馏水,然后滴加紫色石蕊试液(如图Ⅰ),观察到的实验现象是烧杯里的水变成了
紫
紫
色,该实验说明水分子是呈中性
中性
的性质.(选填:酸性,中性,碱性)(2)向(Ⅰ)中的烧杯中再加入稀盐酸,观察到的实验是紫色石蕊试液变成
红
红
色.(3)分别取A、B两个烧杯,A杯中加入蒸馏水,再向其中加入紫色石蕊,B杯中盛有浓盐酸,用一大烧杯把A、B两烧杯的溶液罩在一起(如图Ⅱ),过一段时间后观察到的现象是A烧杯中的紫色石蕊试液变
红色
红色
色.该实验说明构成物质的微粒总是在不断运动
不断运动
.(4)上述实验还说明浓盐酸的两个重要的性质分别是:
①物理性质:浓盐酸具有
挥发
挥发
性②化学性质:浓盐酸具有
酸
酸
性.(选填,酸性或碱性) 如图所示,在一只洁净的小烧杯A中装入30mL蒸馏水,再滴入2-3滴酚酞,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.
如图所示,在一只洁净的小烧杯A中装入30mL蒸馏水,再滴入2-3滴酚酞,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.(1)过一段时间看到的现象是
A烧杯中液体变红
A烧杯中液体变红
,该实验说明分子在不断的运动
不断的运动
.(2)同学们对上述看法不一,有以下两种猜测:
第一种:B烧杯中的蒸馏水使酚酞试液变红
第二种:A烧杯中浓氨水挥发出氨气,扩散到B烧杯中的溶液中使酚酞试液变红.
①你认为哪种猜测正确?
第二种
第二种
②为证明第二种猜测,现设计如下的实验:
| 实验内容、方法 | 观察到的现象 | 结论 |
| 用洁净的小烧杯取20mL水,滴入2-3滴酚酞试液,观察现象 | 不变色 | 水 不能 不能 (填“能”或“不能”,下同)使酚酞变色. |
| 取一张滤纸,滴上酚酞试液,待晾干后,放在装有浓氨水的试剂瓶上方. | 酚酞不变色 | 氨气 不能 不能 使酚酞变色. |
| 将少量氨气通入含有酚酞试液的蒸馏水中 | 溶液变成 红 红 色 |
氨气溶解在水中形成的氨水 能 能 使酚酞变色. |