摘要:24.小明同学在做给液体加热的实验过程中.发现试管破裂了.请你帮他分析一下引起试管破裂的可能原因
网址:http://m.1010jiajiao.com/timu3_id_129926[举报]
 小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.【第一组实验】小明欲证明该双氧水是否失效.
(1)实验过程
①在试管中加入5mL“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
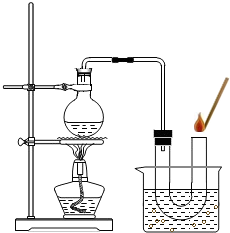
③如右图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是
(2)实验结论:
【第二组实验】小明欲证明二氧化锰在双氧水的分解反应中起催化作用,该物质在反应前后质量是否发生变化.
(1)实验原理
写出化学反应的方程式
(2)实验步骤
①
②将二氧化锰装入大试管中并加入5mL“双氧水”;
③待反应结束后,将大试管里的固体物质进行过滤、洗涤、烘干、称量;
④
(3)做完此实验后,小方认为要证明二氧化锰的催化作用,还需要再补充一个探究实验:探究
【实验反思】依据所做的实验,影响化学反应速率的因素可能有
小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.

第一组实验:小明欲证明该双氧水是否失效.
(1)实验过程
①在试管中加入5mL“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③按图一装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是
(2)实验结论:
第二组实验:小明欲探究Fe2O3能否作为H2O2分解的催化剂,并与MnO2的催化效果进行比较.小明、小李、小张三位同学同时进行H2O2的分解与气体的收集实验.实验时间均以30秒生成气体为准(H2O2均未全部分解)(见图二甲),其他可能影响实验的因素均忽略.相关数据如下:
(1)若50mL量气管中液面的位置如图二乙所示,A与B刻度间相差1mL,刻度A为20,则此时气体的体积为
(2)欲探究Fe2O3在实验中是否起催化作用,首先应比较
还需补充做如下实验(无需写出具体操作步骤):①
实验结论:Fe2O3能加快H2O2的分解,起催化作用.
(3)通过比较Fe2O3 和MnO2 在反应中的反应速率,发现Fe2O3 的催化效果没有二氧化锰好.
查看习题详情和答案>>

第一组实验:小明欲证明该双氧水是否失效.
(1)实验过程
①在试管中加入5mL“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③按图一装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是
冷凝水蒸气
冷凝水蒸气
.(2)实验结论:
双氧水没有失效
双氧水没有失效
.第二组实验:小明欲探究Fe2O3能否作为H2O2分解的催化剂,并与MnO2的催化效果进行比较.小明、小李、小张三位同学同时进行H2O2的分解与气体的收集实验.实验时间均以30秒生成气体为准(H2O2均未全部分解)(见图二甲),其他可能影响实验的因素均忽略.相关数据如下:
| 同学序号 | 质量分数相同的H2O2溶液 | 溶液中加入的物质 | 收集到的气体体积 |
| 小明 | 100ml | 未加其他物质 | a ml |
| 小李 | 100ml | Fe2O3 0.5g | b ml |
| 小张 | 100ml | MnO2 0.5g | c ml |
31.8
31.8
mL.(2)欲探究Fe2O3在实验中是否起催化作用,首先应比较
a
a
和b
b
(选择a、b、c填空)的大小,还需补充做如下实验(无需写出具体操作步骤):①
氧化铁在化学反应前后化学性质是否发生改变
氧化铁在化学反应前后化学性质是否发生改变
;②氧化铁的质量在反应前后是否发生改变
氧化铁的质量在反应前后是否发生改变
.实验结论:Fe2O3能加快H2O2的分解,起催化作用.
(3)通过比较Fe2O3 和MnO2 在反应中的反应速率,发现Fe2O3 的催化效果没有二氧化锰好.
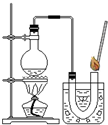 小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.【第一组实验】小明欲证明该双氧水是否失效.
(1)实验过程
①在试管中加入5mL“双氧水”,把带火星的木条伸入试管中,发现木条未复燃;
②用酒精灯给上述试管加热,液体中有气泡产生,把带火星的木条伸入试管中,发现木条仍未复燃;
③如图装置进行操作,带火星的木条复燃,水槽中冰水所起的作用是
冷凝水蒸气
冷凝水蒸气
.(2)实验结论:
双氧水没有失效
双氧水没有失效
.【第二组实验】小明欲证明二氧化锰在双氧水的分解反应中起
催化作用,该物质在反应前后质量是否发生变化.
(1)实验原理
写出化学反应的文字表达式
过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
;| 二氧化锰 |
(2)实验步骤
①
准确称量二氧化锰的质量
准确称量二氧化锰的质量
;②将二氧化锰装入大试管中并加入5mL“双氧水”;
③待反应结束后,将大试管里的固体物质进行过滤、洗涤、烘干、称量;
④
与反应前的质量相比较
与反应前的质量相比较
.(3)做完此实验后,小方认为要证明二氧化锰的催化作用,还需要再补充一个探究实验:探究
二氧化锰在化学反应前后化学性质是否发生改变
二氧化锰在化学反应前后化学性质是否发生改变
.【实验反思】依据所做的实验,影响化学反应速率的因素可能有
温度、催化剂
温度、催化剂
等.【第三组实验】小明利用制得的一瓶氧气,欲验证铁丝能否在氧气中燃烧.
(1)小明先在盛有氧气的集气瓶中加入少量水,目的是
防止生成物熔化后溅落下来炸裂瓶底
防止生成物熔化后溅落下来炸裂瓶底
;(2)小明将用砂纸打磨干净的细铁丝绕成螺旋状,并在一端系上一根火柴,在酒精灯火焰上点燃,待火柴即将燃烧完时,伸入集气瓶中,观察到
剧烈燃烧,火星四射
剧烈燃烧,火星四射
,放出大量热,生成黑色固体
黑色固体
;(3)实验结论:铁丝能在氧气中燃烧,反应的文字表达式为
铁+氧气
四氧化三铁
| 点燃 |
铁+氧气
四氧化三铁
.| 点燃 |
 小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验. 小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.
小明同学在家里的药箱中发现一瓶用来清洗伤口用的消毒液--“双氧水”,他联想到在化学课上曾用过氧化氢溶液制取过氧气,他高兴的将家中的“双氧水”拿到学校的实验室,在老师的指导下和同学们一起做了如下实验.