摘要:17.利用纯净.干燥的氢气还原灼热的氧化铜来测定水的组成.实验装置由A.B.C.D组成(氢气发生装置省略未画出).回答下列问题: (1)如果某学生用锌和较浓的盐酸制取氢气.他用装置A.B是为了得到纯净.干燥的氢气.在装置A中通常盛放 溶液,为了除去 ,在装置B中应盛放的试剂是 .为了除去 . (2)若实验前后.称量结果如下.装氧化铜的玻璃管的质量减少了6.4 g.装氯化钙的U型管的质量增加了7.2 g.根据上述实验数据写出水中氢.氧两种元素质量比的原始计算式 . (3)在装置D中.将CaCl2改换为 .才能检验出氢气还原氧化铜有水生成.
网址:http://m.1010jiajiao.com/timu3_id_12930[举报]
利用纯净、干燥的氢气还原灼热的氧化铜来测定水的组成.实验装置由A、B、C、D、E组成,如图:

请回答下列问题:
①如果某学生用锌和较浓的盐酸制取氢气,他用装置B、C是为了得到纯净、干燥的氢气,他在装置B中通常盛放
②若实验前后,称量结果如下:装氧化铜的玻璃管的质量减少了6.4g,装氯化钙U形管的质量增加了7.2g,根据上述实验数据写出水中氢、氧俩种元素质量比
③在装置E中,将CaCl2改变为
查看习题详情和答案>>

请回答下列问题:
①如果某学生用锌和较浓的盐酸制取氢气,他用装置B、C是为了得到纯净、干燥的氢气,他在装置B中通常盛放
氢氧化钠
氢氧化钠
溶液,为了除去
氯化氢气体
氯化氢气体
;在装置C中盛放的试剂应是
浓硫酸
浓硫酸
,为了除去
水蒸气
水蒸气
.②若实验前后,称量结果如下:装氧化铜的玻璃管的质量减少了6.4g,装氯化钙U形管的质量增加了7.2g,根据上述实验数据写出水中氢、氧俩种元素质量比
1:8
1:8
.③在装置E中,将CaCl2改变为
无水硫酸铜
无水硫酸铜
,才能检验出氢气还原氧化铜有水生成.利用纯净、干燥的氢气还原灼热的氧化铜来测定水的组成.实验装置由A、B、C、D组成(氢气发生装置省略未画出).回答下列问题: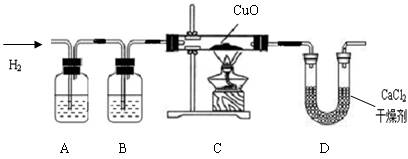
(1如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常放______溶液,其作用是______;在装置B中通常放______溶液,其作用是______.
(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少6、4克,装氯化钙的U型管的质量增加了7、2克.根据上述实验数据,写出水中氢、氧两种元素质量比的原始计算式______.
(3)在装置D中,将CaCl2改换为______,才能检验出氢气还原氧化铜有水生成.
查看习题详情和答案>>
利用纯净、干燥的氢气还原灼热的氧化铜来测定水的组成.实验装置由A、B、C、D组成(氢气发生装置省略未画出).回答下列问题: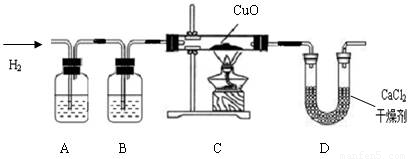
(1如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常放______溶液,其作用是______;在装置B中通常放______溶液,其作用是______.
(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少6、4克,装氯化钙的U型管的质量增加了7、2克.根据上述实验数据,写出水中氢、氧两种元素质量比的原始计算式______.
(3)在装置D中,将CaCl2改换为______,才能检验出氢气还原氧化铜有水生成.
查看习题详情和答案>>

(1如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常放______溶液,其作用是______;在装置B中通常放______溶液,其作用是______.
(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少6、4克,装氯化钙的U型管的质量增加了7、2克.根据上述实验数据,写出水中氢、氧两种元素质量比的原始计算式______.
(3)在装置D中,将CaCl2改换为______,才能检验出氢气还原氧化铜有水生成.
查看习题详情和答案>>
利用纯净、干燥的氢气还原灼热的氧化铜来测定水的组成.实验装置由A、B、C、D组成(氢气发生装置省略未画出).回答下列问题:
(1如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常放______溶液,其作用是______;在装置B中通常放______溶液,其作用是______.
(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少6、4克,装氯化钙的U型管的质量增加了7、2克.根据上述实验数据,写出水中氢、氧两种元素质量比的原始计算式______.
(3)在装置D中,将CaCl2改换为______,才能检验出氢气还原氧化铜有水生成.
查看习题详情和答案>>

(1如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常放______溶液,其作用是______;在装置B中通常放______溶液,其作用是______.
(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少6、4克,装氯化钙的U型管的质量增加了7、2克.根据上述实验数据,写出水中氢、氧两种元素质量比的原始计算式______.
(3)在装置D中,将CaCl2改换为______,才能检验出氢气还原氧化铜有水生成.
查看习题详情和答案>>
38、利用纯净、干燥的氢气还原灼热的氧化铜来测定水的组成.实验装置由A、B、C、D组成(氢气发生装置省略未画出).回答下列问题:
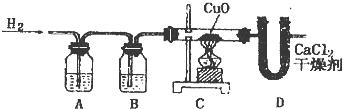
(1)如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常放
(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少6、4克,装氯化钙的U型管的质量增加了7、2克.根据上述实验数据,写出水中氢、氧两种元素质量比的原始计算式
(3)在装置D中,将CaCl2改换为
查看习题详情和答案>>

(1)如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常放
氢氧化钠
溶液,其作用是
吸收氯化氢气体
;在装置B中通常放
浓硫酸
溶液,其作用是
吸收水蒸气
.(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少6、4克,装氯化钙的U型管的质量增加了7、2克.根据上述实验数据,写出水中氢、氧两种元素质量比的原始计算式
(7.2g-6.4g)÷6.4g
.(3)在装置D中,将CaCl2改换为
无水硫酸铜
,才能检验出氢气还原氧化铜有水生成.