摘要:23.如下图.烧杯内盛有水.两个体积相等的集气瓶中 都充满了氧气.夹紧止水夹.并迅速将分别盛有适 量烧着的红磷.硫粉的燃烧匙伸入甲.乙瓶中.塞 紧瓶塞.待燃烧完毕冷却到室温后.打开止水夹. 可见水很快进入 瓶中.原因是 .
网址:http://m.1010jiajiao.com/timu3_id_127242[举报]
下面两个实验的原理有相似之处.请回答问题:
A.按如图1组装仪器,关闭止水夹,通电使红磷燃烧.
(1)燃烧的现象是
(2)红磷燃烧一段时间后,自动熄灭了,你认为原因 是
(3)冷却后,松开止水夹,你观察到的现象为
B.如图2是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验.请完成实验报告:
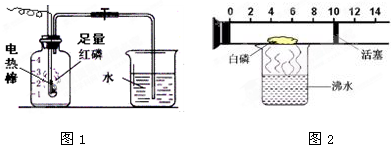
(1)实验目的:测定空气中
(2)实验现象:白磷着火燃烧,活塞先向右移,后向左移,最后停在刻度约为
(3)实验结论:
查看习题详情和答案>>
A.按如图1组装仪器,关闭止水夹,通电使红磷燃烧.
(1)燃烧的现象是
产生黄白色火焰,产生白烟,火焰慢慢熄灭
产生黄白色火焰,产生白烟,火焰慢慢熄灭
.(2)红磷燃烧一段时间后,自动熄灭了,你认为原因 是
集气瓶内的氧气已消耗完
集气瓶内的氧气已消耗完
.(3)冷却后,松开止水夹,你观察到的现象为
烧杯里的水倒吸到集气瓶内,集气瓶中的水约占集气瓶容积
| 1 |
| 5 |
烧杯里的水倒吸到集气瓶内,集气瓶中的水约占集气瓶容积
.| 1 |
| 5 |
B.如图2是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验.请完成实验报告:

(1)实验目的:测定空气中
氧气
氧气
的含量.(2)实验现象:白磷着火燃烧,活塞先向右移,后向左移,最后停在刻度约为
8
8
(填整数)的位置上.(3)实验结论:
空气中,氧气约占空气体积的
| 1 |
| 5 |
空气中,氧气约占空气体积的
.| 1 |
| 5 |
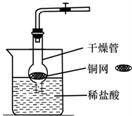 27、CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
27、CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:(1)该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如右图所示.在干燥管内的铜网上应盛放
石灰石(或大理石)
;若将铜网换成铁网,可能产生的后果是铁网被腐蚀,制得的CO2气体中混有H2
,其原因是(用化学方程式表示)Fe+2HCl═FeCl2+H2↑
.(2)该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?
①小明设计了甲、乙两个实验来验证C02与NaOH发生了化学反应,如图所示.实验现象为:甲--软塑料瓶变瘪,乙--“瓶吞鸡蛋”.
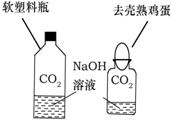
小虎同学认为上述实验是可行的.其共同原理是
氢氧化钠溶液和二氧化碳反应导致瓶内压强减小
.小雯同学提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应.其理由是
二氧化碳能溶于水,也能使瓶内压强减小
.小明同学针对小雯的质疑又补充了一个对照实验,这个实验是
把瓶内的氢氧化钠溶液换成等体积的水,做对比实验
.②小虎向甲实验后变瘪塑料瓶的溶液中加入
稀盐酸
,观察到有气泡产生
现象,从而证明CO2与NaOH已经发生了反应. 用来测定空气成分的方法有很多,课本上就是用红磷在空气中燃烧的测定方法.实验过程有:
用来测定空气成分的方法有很多,课本上就是用红磷在空气中燃烧的测定方法.实验过程有:①点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧;
②将集气瓶容积划分五份,并做好标记,
③待冷却至室温后,打开弹簧夹,观察现象.
试回答以下问题:
(1)将实验过程正确排序:
②①③
②①③
.(2)整个实验过程中,看见的现象主要有:
产生大量的白烟;
产生大量的白烟;
;待红磷熄灭并冷却后,打开弹簧夹,水顺着导管流入集气瓶,且水的体积占集气瓶总容积的
| 1 |
| 5 |
待红磷熄灭并冷却后,打开弹簧夹,水顺着导管流入集气瓶,且水的体积占集气瓶总容积的
.| 1 |
| 5 |
(3)写出红磷燃烧的化学反应式
4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
.
| ||
(4)此实验成功的关键有:
①红磷要足量
②导管内要注满水
③要冷却到室温后再打开弹簧夹,
还有最关键的一点是
要保证实验装置密封
要保证实验装置密封
(5)有人认为预先在集气瓶中装入一定量的水更好,这样做的目的是
防止燃烧生成的高温固体炸裂集气瓶
防止燃烧生成的高温固体炸裂集气瓶
(6)还有人认为可以用如图所示装置来测定.在一个具有刻度和可以左右滑动的玻璃容器里放一粒白磷(适量)(白磷燃烧所需最低温度为40℃),将玻璃容器固定好,放在盛有80℃热水的烧杯上.如图所示,试回答:
①实验一开始,可以看见活塞向
右
右
(填“左”还是“右”)移动,原因是装置内的气体受热体积会膨胀
装置内的气体受热体积会膨胀
②实验结束并恢复到常温后,活塞应该停在刻度
4
4
处.(7)两个实验均可得出的重要结论是
空气中氧气约占空气体积的
| 1 |
| 5 |
空气中氧气约占空气体积的
.| 1 |
| 5 |
 24、经过一年的化学学习,我们亲身体验了一系列的探究实验,感受了化学的无穷魅力.小强在回顾整理下列实验中提炼了许多探究的方法.
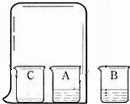
24、经过一年的化学学习,我们亲身体验了一系列的探究实验,感受了化学的无穷魅力.小强在回顾整理下列实验中提炼了许多探究的方法.实验一、探究分子在不断运动(如右图)
实验现象:
B烧杯中的无色酚酞溶液变红
.该实验的探究方法是:对看不见、摸不着的粒子,要“观察”它的运动可以设计实验,通过宏观的现象来间接认识.
实验二、探究二氧化碳与水的反应(取四朵用紫色石蕊溶液染成紫色的干燥的小花,进行下图所示实验)

实验现象:(Ⅰ)、(Ⅳ)中的小花变红.
设计(Ⅱ)、(Ⅲ)实验的目的是:
验证水和二氧化碳分别是否能使紫色石蕊变色
.该实验的探究方法是:设计分析
B
(填“A”或“B”或“C”),获得结论.A.仅一个单因素的实验B.有多种因素的对比实验C.用前面实验的生成物继续实验
实验三、验证二氧化碳与氢氧化钠溶液确实发生了反应(实验如下表所示)
| 方案 | 实验步骤 | 实验现象 |
| 1 | 取两个等体积的软塑料瓶,充满二氧化碳,然后 . |
|
| 2 | 先将二氧化碳通入盛有足量氢氧化钠溶液的试管 中,然后. |
通过密闭容器内气体压强变化的程度的对比来判断反应的发生(或通过反应物量的减少来判断反应的发生).
,方案2的探究方法是
通过验证生成物的存在来判断反应的发生
.小结:上述三个实验告诉我们:当某些化学反应现象不明显或不足以说明问题时,要千方百计通过设计出具有明显现象的实验,来准确推知和认识化学反应.
 化学是一门实验科学.我们可以通过观察肉眼可见的实验现象,再加上分析推理,来认识分子的性质和确认分子的真实存在.
化学是一门实验科学.我们可以通过观察肉眼可见的实验现象,再加上分析推理,来认识分子的性质和确认分子的真实存在.