摘要:公式:Q=Q有+Q无.Q总=Q有/η 例4.在一把质量为500g的铝质电热水壶中.装有2kg水.用这把电水壶把20℃的水加热到100℃.若该电水壶的热效率为80%.问烧开这壶水需要消耗多少电能?[C铝=0.88×103J/.C水=4.2×103J/] 分析:本题与例2的区别在于消耗电能并没有全部被水吸收.壶身.外界空气等均要吸热.只有水吸收热量为有效部分.空气吸热未知.所以不能用Q=Q有+Q无计算.因为知道电水壶的热效率η.所以可使用Q总=Q有/η计算.而不需要计算铝壶吸收的热量. 解:Q水=C水m =4.2×103×2× =6.72×105(J) Q=-=-=8.4×105(J) 答略
网址:http://m.1010jiajiao.com/timu3_id_123836[举报]
印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:2FeCl3+Cu=2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 ( )
| A.烧杯中有铜无铁 | B.烧杯中有铁无铜 |
| C.烧杯中铁、铜都有 | D.烧杯中铁、铜都无 |
印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:2FeCl3+Cu=2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是??? (? )
? A.烧杯中有铜无铁?? B.烧杯中有铁无铜
? C.烧杯中铁、铜都有??? D.烧杯中铁、铜都无
查看习题详情和答案>>
印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:
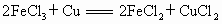 ,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
[
]|
A .烧杯中有铜无铁 |
B .烧杯中有铁无铜 |
|
C .烧杯中铁、铜都有 |
D .烧杯中铁、铜都无 |
印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:
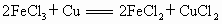 ,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
[
]|
A .烧杯中有铜无铁 |
B .烧杯中有铁无铜 |
|
C .烧杯中铁、铜都有 |
D .烧杯中铁、铜都无 |