摘要:① Ba2++SO42-=BaSO4↓ ②Ag++Cl-=AgCl↓ ③除K+.Na+外的金属离子+CO3-=难溶性碳酸盐↓ ④除K+.Na+.Ca+.Ba+外的金属离子+OH-=难溶性碱↓16.有关不同 1.金刚石和石墨的物理性质不同:是因为 碳原子排列不同. 2.生铁和钢的性能不同:是因为 含碳量不同. 3.一氧化碳和二氧化碳的化学性质不同:是因为 分子构成不同. (氧气和臭氧的化学性质不同是因为分子构成不同,水和双氧水的化学性质不同是因为分子构成不同.) 4.元素种类不同:是因为质子数不同. 5.元素化合价不同:是因为最外层电子数不同. 6.钠原子和钠离子的化学性质不同:是因为最外层电子数不同
网址:http://m.1010jiajiao.com/timu3_id_123556[举报]
仔细观察下列微观示意图,回答有关问题:
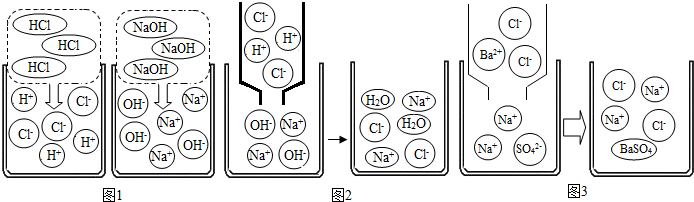
(1)图1是HCl和NaOH在水中解离出离子的示意图,HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推BaCl2在水中会解离出的离子是
(2)图2是氢氧化钠溶液与盐酸反应的微观示意图,该反应的实质是H++OH-→H2O,图3是氯化钡溶液与硫酸钠溶液反应的微观示意图,该反应的实质是
查看习题详情和答案>>

(1)图1是HCl和NaOH在水中解离出离子的示意图,HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推BaCl2在水中会解离出的离子是
Ba2+和Cl-
Ba2+和Cl-
,Na2SO4在水中会解离出的离子是Na+和SO42-
Na+和SO42-
.(2)图2是氢氧化钠溶液与盐酸反应的微观示意图,该反应的实质是H++OH-→H2O,图3是氯化钡溶液与硫酸钠溶液反应的微观示意图,该反应的实质是
Ba2++SO42-=BaSO4↓
Ba2++SO42-=BaSO4↓
.由此类推,碳酸钠溶液和稀硫酸反应的实质是2H++CO32-=H2O+CO2↑
2H++CO32-=H2O+CO2↑
.(2010?南宁)某校化学兴趣小组的同学学习了酸、碱、盐的知识后,对课本中“酸、碱、盐之间并不是都能发生复分解反应”这句话产生了兴趣,展开了探究性学习.
(1)【提出问题】发生复分解反应应具备哪些条件?
(2)【活动探究】该小组同学进行以下四组实验,发现均能反应,写出反应④的化学方程式:
①硝酸钡溶液与稀硫酸 ②稀硫酸与碳酸钾溶液 ③稀盐酸与氢氧化钠溶液 ④硝酸钡溶液与碳酸钾溶液:
(3)【理论分析】上述反应未什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如:
①中有Ba2++SO42-→BaSO4↓ ②中有H++CO32-→H2O+CO2↑ ③中有H++OH-→H2O ④中有
(4)【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或水,是判断酸、碱、盐之间能否发生复分解反应的主要条件.
(5)【形成网络】按照一定的顺序排列某些离子,就可以形成一种知识网络.在网络中,用“--”相连接的阴、阳离子间能两两结合生成沉淀或气体或水.现有Ca2+、HCO3-两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络.
”内,使其形成一个更为完整的复分解反应的知识网络.
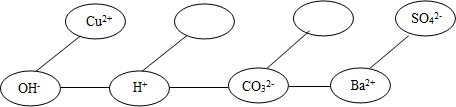
(6)【拓展应用】根据得出的结论,解决以下问题:
已知t℃时四种化合物在溶剂A和溶剂B中各自的溶解度(g/100g溶剂)如下表所示.
t℃时表中四种化合物在溶剂A中发生复分解反应的化学方程式为:BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2
则表中四种化合物中某两种化合物在溶剂B中能发生复分解反应的化学方程式为:
查看习题详情和答案>>
(1)【提出问题】发生复分解反应应具备哪些条件?
(2)【活动探究】该小组同学进行以下四组实验,发现均能反应,写出反应④的化学方程式:
①硝酸钡溶液与稀硫酸 ②稀硫酸与碳酸钾溶液 ③稀盐酸与氢氧化钠溶液 ④硝酸钡溶液与碳酸钾溶液:
Ba(NO3)2+K2CO3═BaCO3↓+2KNO3
Ba(NO3)2+K2CO3═BaCO3↓+2KNO3
.(3)【理论分析】上述反应未什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如:
①中有Ba2++SO42-→BaSO4↓ ②中有H++CO32-→H2O+CO2↑ ③中有H++OH-→H2O ④中有
Ba2++CO32-→BaCO3↓
Ba2++CO32-→BaCO3↓
两种离子,所以才发生化学反应.(4)【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或水,是判断酸、碱、盐之间能否发生复分解反应的主要条件.
(5)【形成网络】按照一定的顺序排列某些离子,就可以形成一种知识网络.在网络中,用“--”相连接的阴、阳离子间能两两结合生成沉淀或气体或水.现有Ca2+、HCO3-两种离子,请将它们填入下面合适的“
 ”内,使其形成一个更为完整的复分解反应的知识网络.
”内,使其形成一个更为完整的复分解反应的知识网络.
(6)【拓展应用】根据得出的结论,解决以下问题:
已知t℃时四种化合物在溶剂A和溶剂B中各自的溶解度(g/100g溶剂)如下表所示.
| 物质 | 在溶剂A中的溶解度 | 在溶剂B中的溶解度 |
| AgNO3 | 170 | 86 |
| Ba(NO3)2 | 9.3 | 97.2 |
| AgCl | 1.5×10-4 | 0.8 |
| BaCl2 | 33.3 | 约为0 |
则表中四种化合物中某两种化合物在溶剂B中能发生复分解反应的化学方程式为:
Ba(NO3)2+2AgCl=BaCl2↓+2AgNO3
Ba(NO3)2+2AgCl=BaCl2↓+2AgNO3
.
某中学同学学完第十一单元后,在教师的指导下对“酸、碱、盐之间并不是都能发生复分解反应,发生复分解反应应具备哪些条件?”设计了如下科学探究活动.
(1)提出问题:发生复分解反应应具备哪些条件?
(2)猜想与假设:①酸、碱、盐的溶液混和后溶液中自由移动的离子变少了,反应就发生了;②酸、碱、盐的溶液混和后,肉眼能看到新物质的产生(例如,有沉淀或气体),反应才发生.
(3)进行实验并观察实验现象,请结合实验完成下表:
(4)解释与结论:
上述反应为什么能够发生?是因为在这些反应物中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如①中有Ba2++SO42-→BaSO4↓,②中有H++CO32-→H2O+CO2↑,③中有H++OH-→H2O,④中有 ,⑤中有 ,从而使化学反应得以发生.经过分析,同学们得出的结论,猜想 正确.
(5)形成网络:按照一定的顺序排列某些离子,就可以形成一个知识网络.在网络中,用“---”相连接的阴、阳离子之间能两两结合生成沉淀或气体或水.现有Ca2+、HCO3-、NH4+三种离子,请将它们填入合适的“ ”内,使其形成一个更完整的复分解反应的知识网络.
”内,使其形成一个更完整的复分解反应的知识网络.

(6)拓展应用:根据得出的结论,解决以下问题:
t℃时四种化合物在溶剂A和溶剂B的溶解度如下表:
t℃时表中四种化合物在溶剂A中发生复分解反应的化学方程式为BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2,则表中四种化合物中某两种化合物在溶剂B中发生复分解反应的化学方程式为 .
查看习题详情和答案>>
(1)提出问题:发生复分解反应应具备哪些条件?
(2)猜想与假设:①酸、碱、盐的溶液混和后溶液中自由移动的离子变少了,反应就发生了;②酸、碱、盐的溶液混和后,肉眼能看到新物质的产生(例如,有沉淀或气体),反应才发生.
(3)进行实验并观察实验现象,请结合实验完成下表:
| 实验步骤 | 实验现象 | 化学反应方程式 |
| ①硝酸钡溶液中滴加稀硫酸 | H2SO4+Ba(NO3)2=BaSO4↓+2HNO3 | |
| ②稀硫酸溶液中滴加碳酸钾溶液 | H2SO4+K2CO3=K2SO4+CO2↑+H2O | |
| ③稀盐酸溶液中先加2滴酚酞试液再滴加氢氧化钠溶液 | 溶液由无色变浅红色,并不褪色 | |
| ④硝酸钡溶液中滴加碳酸钾溶液 | 有白色沉淀 | |
| ⑤氯化铵溶液中滴加浓氢氧化钠溶液后加热,并用湿的红石蕊试纸检验生成的气体 | 有无色、刺激性气味的气体生成,该气体能使湿的红石蕊试纸变蓝 |
上述反应为什么能够发生?是因为在这些反应物中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如①中有Ba2++SO42-→BaSO4↓,②中有H++CO32-→H2O+CO2↑,③中有H++OH-→H2O,④中有
(5)形成网络:按照一定的顺序排列某些离子,就可以形成一个知识网络.在网络中,用“---”相连接的阴、阳离子之间能两两结合生成沉淀或气体或水.现有Ca2+、HCO3-、NH4+三种离子,请将它们填入合适的“
 ”内,使其形成一个更完整的复分解反应的知识网络.
”内,使其形成一个更完整的复分解反应的知识网络.
(6)拓展应用:根据得出的结论,解决以下问题:
t℃时四种化合物在溶剂A和溶剂B的溶解度如下表:
| 物质 | 在溶剂A中的溶解度/g | 在溶剂B中的溶解度/g |
| AgNO3 | 170 | 86 |
| Ba(NO3)2 | 9.3 | 97.2 |
| AgCl | 1.5×10-4 | 0.8 |
| BaCl2 | 33.3 | 约为0 |
24、有6瓶白色固体试剂,分别是氯化钡、氢氧化钠、硫酸钠、硫酸铵、无水硫酸铜、碳酸钠.现只提供蒸馏水,通过下面的实验步骤即可鉴别它们.请填写下列空白:
(1)各取适量固体试剂分别加入6支试管中,加入适量蒸馏水,振荡试管,观察到的现象是:
被检出的物质的化学式(分子式)是
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式是:
被检出的物质的化学式(分子式)是
(3)鉴别余下未检出物质的方法和观察到的现象是:
查看习题详情和答案>>
(1)各取适量固体试剂分别加入6支试管中,加入适量蒸馏水,振荡试管,观察到的现象是:
6种固体全部溶解,5支试管中得到无色溶液,1支试管中得到蓝色溶液
.被检出的物质的化学式(分子式)是
CuSO4
.(2)分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式是:
1支试管中有白色沉淀生成,Ba2++SO42-═BaSO4↓,2支试管中有蓝色沉淀生成,
Cu2++2OH-=Cu(OH)2↓,Cu2++CO32-=CuCO3↓
Cu2++2OH-=Cu(OH)2↓,Cu2++CO32-=CuCO3↓
被检出的物质的化学式(分子式)是
BaCl2
(3)鉴别余下未检出物质的方法和观察到的现象是:
(ⅰ)分别取(2)中能产生蓝色沉淀的两种溶液,向其中加入BaCl2溶液,有白色沉淀生成的是Na2CO3溶液,无沉淀生成的是NaOH溶液;
(ⅱ)分别取少量未检出的溶液,往其中加入NaOH溶液,无明显现象的是Na2SO4溶液,有刺激性气味气体产生的是(NH4)2SO4溶液.
.(ⅱ)分别取少量未检出的溶液,往其中加入NaOH溶液,无明显现象的是Na2SO4溶液,有刺激性气味气体产生的是(NH4)2SO4溶液.