摘要: 表格数据分析型计算题 例2. 某同学去我市的道场山风景区游玩时.取回了若干块矿石样品.它采用了以下的方法对样品中碳酸钙的质量分数进行检测:取这种石灰石样品6g.把40g稀盐酸分四次加入.测量过程所得数据见下表(已知石灰石样品中的杂质不溶于水.不与盐酸反应).求: (1)6g石灰石样品中含有的杂质为 , 样品中CaCO3的质量分数,(4)所用稀盐酸的质量分数. 解析:解答本题的关键是分析表中所给数据之间的关系.并做出正确的判断.(1)通过表中次序3和次序4的数据比较.可判断此时的石灰石中CaCO3已完全反应.且其中所含杂质的质量为0.6g.所含CaCO3的质量为:6g-0.6g=5.4g,(2)第一次加入10g盐酸.反应后剩余固体的质量为4.0g.说明10g盐酸消耗了2g CaCO3.因此第二次加入10g盐酸后所消耗CaCO3的质量共为4g.,(3)样品中CaCO3的质量分数为:5.4g/6g×100%=90%. (4)设所用稀盐酸的质量分数为x. 100 73 2g 10g·x (提示:计算稀盐酸的溶质质量分数时.只能用前两次所用盐酸中的任一次.不能根据第三次或第四次盐酸的质量计算.因为这两次盐酸有剩余.) 答:(1)6g石灰石样品中含有的杂质为0.6g,样品中CaCO3的质量分数为90%,(4)所用稀盐酸的质量分数为14.6%.
网址:http://m.1010jiajiao.com/timu3_id_123541[举报]
(2012?镇江)工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下的实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O4?3H2O)在浓硫酸作用下受热分解,化学方程式为:
H2C2O4?3H2O
CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是
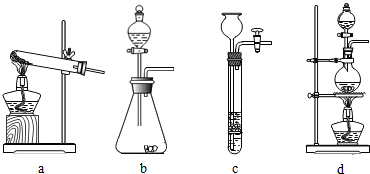
【问题讨论】用下图所示装置进行实验:
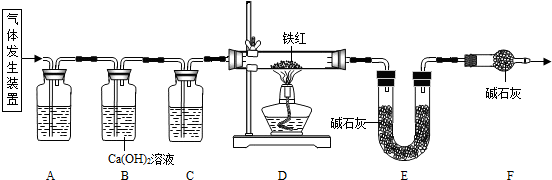
(2)实验前应先
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是
a.浓硫酸 b.澄清石灰水 c.氢氧化钠溶液
(4)B装置的作用是
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前
(6)写出D装置中所发生反应的一个化学方程式
【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数:
(7)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为mg,则
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是
【实验反思】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会
反思2:请指出【问题讨论】中实验装置的一个明显缺陷
查看习题详情和答案>>
【资料1】草酸晶体(H2C2O4?3H2O)在浓硫酸作用下受热分解,化学方程式为:
H2C2O4?3H2O
| 浓硫酸 |
| △ |
(1)下列可用作草酸分解制取气体的装置是
d
d
(填字母编号)
【问题讨论】用下图所示装置进行实验:

(2)实验前应先
检查装置的气密性
检查装置的气密性
.(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是
c
c
、a
a
(填字母编号)a.浓硫酸 b.澄清石灰水 c.氢氧化钠溶液
(4)B装置的作用是
验证二氧化碳已除尽
验证二氧化碳已除尽
.(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前
将装置中的空气排出,防止发生爆炸
将装置中的空气排出,防止发生爆炸
.停止加热后驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收
驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收
.(6)写出D装置中所发生反应的一个化学方程式
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
【数据分析与计算】
【资料2】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为mg,则
7.0
7.0
<m<7.78
7.78
.②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是
76.0%
76.0%
.【实验反思】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会
偏小
偏小
(填“偏小”、“不变”或“偏大”).反思2:请指出【问题讨论】中实验装置的一个明显缺陷
缺少尾气处理装置
缺少尾气处理装置
.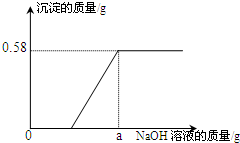 (2013?顺德区质检)某环保小组监测到化工厂排放的废水中含有盐酸和氯化镁两种污染物,为测定该废水中各污染物的含量,环保小组进行了以下实验:
(2013?顺德区质检)某环保小组监测到化工厂排放的废水中含有盐酸和氯化镁两种污染物,为测定该废水中各污染物的含量,环保小组进行了以下实验:【实验一】取废水100g,向其中加入溶质质量分数为10%的氢氧化钠溶液.测得沉淀质量与所加入氢氧化钠溶液质量的关系如图.请根据实验及有关数据分析和计算:
(1)向100g该废水中加入足量的氢氧化钠溶液时,产生的沉淀质量为
0.58
0.58
g.(2)求该废水中氯化镁溶质的质量分数是多少?
【实验二】取三份废水各100g,分别缓慢加入到20g、40g和60g某硝酸银溶液中,测得三组实验数据见下表:
| 第一组 | 第二组 | 第三组 | |
| 硝酸银溶液的质量/g | 20 | 40 | 60 |
| 生成沉淀的质量/s | 2.870 | 5.740 | 7.175 |
50
50
g时,可恰好完全反应.(4)【实验一】图示中,a的数值为
24
24
.某环保小组监测到化工厂排放的废水中含有盐酸和氯化镁两种污染物,为测定该废水中各污染物的含量,环保小组进行了以下实验:
【实验一】取废水100g,向其中加入溶质质量分数为10%的氢氧化钠溶液。测得沉淀质量与所加入氢氧化钠溶液质量的关系如图。请根据实验及有关数据分析和计算: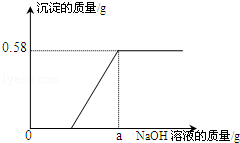
(1)向100g该废水中加入足量的氢氧化钠溶液时,产生的沉淀质量为 g。
(2)求该废水中氯化镁溶质的质量分数是多少?
【实验二】取三份废水各100g,分别缓慢加入到20g、40g和60g某硝酸银溶液中,测得三组实验数据见下表:
| | 第一组 | 第二组 | 第三组 |
| 硝酸银溶液的质量/g | 20 | 40 | 60 |
| 生成沉淀的质量/s | 2.870 | 5.740 | 7.175 |
(3)100g废水中加入硝酸银溶液的质量为 g时,可恰好完全反应。
(4)【实验一】图示中,a的数值为 。 查看习题详情和答案>>
某环保小组监测到化工厂排放的废水中含有盐酸和氯化镁两种污染物,为测定该废水中各污染物的含量,环保小组进行了以下实验:
【实验一】取废水100g,向其中加入溶质质量分数为10%的氢氧化钠溶液。测得沉淀质量与所加入氢氧化钠溶液质量的关系如图。请根据实验及有关数据分析和计算:

(1)向100g该废水中加入足量的氢氧化钠溶液时,产生的沉淀质量为 g。
(2)求该废水中氯化镁溶质的质量分数是多少?
【实验二】取三份废水各100g,分别缓慢加入到20g、40g和60g某硝酸银溶液中,测得三组实验数据见下表:
|
|
第一组 |
第二组 |
第三组 |
|
硝酸银溶液的质量/g |
20 |
40 |
60 |
|
生成沉淀的质量/s |
2.870 |
5.740 |
7.175 |
(3)100g废水中加入硝酸银溶液的质量为 g时,可恰好完全反应。
(4)【实验一】图示中,a的数值为 。
查看习题详情和答案>>
