网址:http://m.1010jiajiao.com/timu3_id_123353[举报]
| 烧杯1 | 烧杯2 | 烧杯3 | 烧杯4 | 烧杯5 | |
| 加入样品的质量/克 | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/克 | 10 | 20 | 30 | 40 | 50 |
| 充分反应后生成气体的质量/克 | 0.88 | 1.76 | 2.64 | 3.52 | 3.52 |
(2)求样品中碳酸钙的质量分数.
以下是常见的实验装置图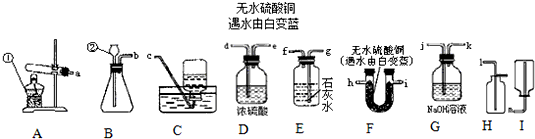
(1)图中有标号的仪器名称是:①________ ②________
(2)制取并收集干燥的CO2气体,选用的装置组合是________(填装置字母代号,下同),检验是否收集满的方法是________.制取该气体的化学方程式是________;小明建议将稀盐酸换成浓盐酸,你认为此方法可行吗?________(填“可行”或“不可行”),理由是________.
(3)某化学研究性小组的同学选用上述装置对常见化肥进行了探究:
碳酸氢铵(NH4HCO3)是一种常见的________肥,受热易分解生成三种化合物,其中一种是氨气(NH3),另两种可能是________、________;为了证明此猜想,选择上述部分装置,各接口的连接顺序是a接________接________接________.
(4)如用H2O2和MnO2制氧气,应选用________作为发生装置,其化学反应方程式为________.
对此实验,让我们继续思考并研究几个问题:
问题①:催化剂MnO2的用量对反应速率有没无影响,我的实验方案是:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| MnO2粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用时间(t) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 |
答:________.
问题②:H2O2溶液的溶质质量分数对反应速率有没有影响,你的实验方案是:
答:________.
问题③:还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:________.
问题④:已知氧气在该实验条件下的密度为1.28g/L,若要制取250mL氧气,计算理论上至少需要消耗30%的H2O2溶液多少克?(相对原子质量:H-1O-16) 查看习题详情和答案>>
酸、碱溶液是化学常见的物质,依据所给内容回答问题:
下表是在不 同温度下氢氧化钠的溶解度:
同温度下氢氧化钠的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31 | 91 | 111 | 129 | 313 | 336 |
(1)氢氧化钠溶液中的溶质是 。20℃时,向100克水中加入100克氢氧化钠固体,所得溶液为 溶液(填“饱和”或“不 饱和”),其溶液的质量是 克。
饱和”),其溶液的质量是 克。
(2)在学习过程中,可以判断反应发 生的方法有多种。
生的方法有多种。
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
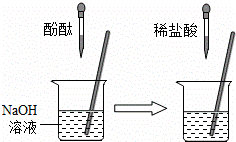
②在右图的实验中,当观察到的现象是
就可证明NaOH与HCl发生了反应。
③不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 。
查看习题详情和答案>>酸、碱溶液是化学常见的物质,依据所给内容回答问题:
下表是在不 同温度下氢氧化钠的溶解度:
同温度下氢氧化钠的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31 | 91 | 111 | 129 | 313 | 336 |
(1)氢氧化钠溶液中的溶质是 。20℃时,向100克水中加入100克氢氧化钠固体,所得溶液为 溶液(填“饱和”或“不 饱和”),其溶液的质量是 克。
饱和”),其溶液的质量是 克。
(2)在学习过程中,可以判断反应发 生的方法有多种。
生的方法有多种。
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
②在右图的实验中,当观察到的现象是
就可证明NaOH与HCl发生了反应。
③不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 。
查看习题详情和答案>>酸、碱溶液是化学常见的物质,依据所给内容回答问题:
下表是在不同温度下氢氧化钠的溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31 | 91 | 111 | 129 | 313 | 336 |
(1)氢氧化钠溶液中的溶质是 .20℃时,向100克水中加入100克氢氧化钠固体,所得溶液为 溶液(填“饱和”或“不饱和”),其溶液的质量是 克.
(2)在学习过程中,可以判断反应发生的方法有多种.
①向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
当加入氢氧化钠溶液的体积为 mL时,稀盐酸和氢氧化钠溶液恰好完全反应.
②在如图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应.
③不使用指示剂或pH试纸等方法,也可证明反应发生.向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是 .