摘要:5.能源的划分有多种方法.来自自然界.没有经过任何加工或转换的能源叫做一次能源,从一次能源直接或间接转化而来的能源叫做二次能源.请把下列九种能源按要求填入下面空格.并指出哪些是不可再生能源. 煤.石油.水力.汽油.酒精.天然气.煤气.风力.电 一次能源: 二次能源: 不可再生能源:
网址:http://m.1010jiajiao.com/timu3_id_120590[举报]
 (2009?杭州)
(2009?杭州)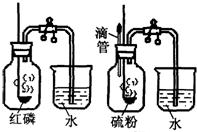 “空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图所示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:(1)、反应结束后,打开铁夹,水自动注入集气瓶的直接原因是
装置内的压强小于外界的气压
装置内的压强小于外界的气压
.(2)、乙生也设计了一个如图所示的实验方案,装置和操作同甲类似,只不过用硫粉代替了红磷,并增加了滴管.要使实验成功,乙在滴管中应加入
氢氧化钠(其他碱也可)
氢氧化钠(其他碱也可)
溶液.并反应后滴入,写出该溶液发生反应的化学方程式SO2+2NaOH=Na2SO3+H2O
SO2+2NaOH=Na2SO3+H2O
.(3)、若空气中氮气也能和红磷反应,能否用该方法来测定空气中氧气的含量?
不能
不能
.(4)、丙生想利用氧气和某种金属的反应,来测定空气中的氧气含量.他选择利用下列仪器、药品:①带瓶塞的l000ml烧瓶②电子天平(称量精度为0.01克)③酒精灯④某种金属粉末.他的实验步骤如下:准确称量某种金属粉末的质量(足量),将其放入烧瓶,塞紧瓶塞,放置一段时间后,倒出烧瓶中粉末,并称其质量.写出丙生的实验思路
借助金属反应消耗氧气引起的质量变化,从而求出氧气的体积,最终求出空气中氧气的含量
借助金属反应消耗氧气引起的质量变化,从而求出氧气的体积,最终求出空气中氧气的含量
.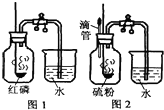 “空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:(1)图1反应结束后,打开铁夹,水自动注入集气瓶的直接原因是
氧气的消耗导致装置内的压强减小
氧气的消耗导致装置内的压强减小
.(2)乙生也设计了一个如图2所示的实验方案,装置和操作同甲类似,只不过用硫粉代替了红磷,并增加了滴管.要使实验成功,乙在滴管中应加入
氢氧化钠
氢氧化钠
溶液.(3)该实验我们可得出氧气约占空气体积
| 1 |
| 5 |
| 1 |
| 5 |
| 4 |
| 5 |
氮气
氮气
,该气体具有的化学性质是不燃烧、不支持燃烧
不燃烧、不支持燃烧
.(4)若空气中氮气也能和红磷反应,能否用该方法来测定空气中氧气的含量?
不能
不能
.(填:“能”或“不能”) 28、“空气中氧气含量的测定”有多种方法.
28、“空气中氧气含量的测定”有多种方法.(1)甲同学设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水自动注入集气瓶.
①红磷在空气中燃烧的现象是
产生大量白烟
.②水自动注入集气瓶的原因是
氧气被消耗,生成的五氧化二磷为固体,集气瓶内的气体压强小于瓶外大气压强
.(2)乙同学设计了如图2所示的实验方案:装置和操作与甲类似,只是用硫粉代替了红磷,并增加了一支滴管,滴管中装有少量的某种溶液.实验中待硫燃烧的火焰熄灭,集气瓶冷却至室温,打开铁夹,水却没有自动注入集气瓶.为使实验成功,乙同学将滴管中的溶液挤入集气瓶,观察到水又自动注入集气瓶.滴管中最适宜盛装
NaOH
溶液,它的作用是2NaOH+SO2═Na2SO3+H2O
(用化学方程式表示).(3)丙同学想利用氧气和某种金属的反应,来测定空气中的氧气含量.他选择了下列仪器和药品:带瓶塞的l000mL烧瓶、电子天平(称量精度为0.001g)、酒精灯、若干片某种金属等.
①他的实验步骤如下:
a.准确称量某种金属片的质量(足量),将其放入烧瓶,塞紧瓶塞;
b.将烧瓶置于火焰上加热足够长时间后,再冷却到室温;
c.倒出烧瓶中的片状固体,然后
称量这些片状固体的质量
;d.计算.
②用酒精灯给烧瓶加热时还应同时使用铁架台(含铁夹、铁圈)、
石棉网
(填仪器名称).③为保证实验的成功,丙同学可以选用以下哪一种金属片?
B
(选填序号).A.铝片 B.铜片 C.金片
(4)丁同学建议丙同学也可以用镁条代替上述选定的金属来测定空气中的氧气含量,从保护仪器的角度看你认为此建议
不合理
(选填“合理”或“不合理”),理由是镁条燃烧时放出的大量热可能导致烧瓶底受热不均匀而炸裂
.金属镁和镁合金在航空、汽车制造和电子工业等领域具有广泛的用途,金属镁的冶炼有多种方法,其中之一为皮江法.该方法是以白云石(CaCO3?MgCO3)为原料,经高温煅烧生成氧化物(CaO?MgO),氧化物在还原炉中经1200℃真空条件下用硅铁(硅铁含硅量达95%--99%)还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁.反应工艺流程如下图:

(1)写出还原炉中硅铁还原氧化镁发生置换反应的化学方程式
(2)在冶炼过程中反应温度对生成金属镁的影响如图,从图中分析,该还原反应属于
(3)还原炉中需要在1200℃真空条件下反应,反应达到平衡时的温度与压强的关系如下
真空条件对制备金属镁来讲,可以达到的目的是:①
(4)含镁矿物常见的有菱镁矿(MgCO3)、白云石和光卤石(KCl?MgCl2?6H2O),其中
KCl?MgCl2?6H2O属于
A.盐 B.混合物
(5)写出煅烧白云石的反应化学方程式
查看习题详情和答案>>

(1)写出还原炉中硅铁还原氧化镁发生置换反应的化学方程式
2MgO+Si
2Mg↑+SiO2
| ||
2MgO+Si
2Mg↑+SiO2
| ||
(2)在冶炼过程中反应温度对生成金属镁的影响如图,从图中分析,该还原反应属于
吸热
吸热
(填“吸热”“放热”)反应,理由是升高温度Mg的产率增大,说明反应是吸热反应
升高温度Mg的产率增大,说明反应是吸热反应
.(3)还原炉中需要在1200℃真空条件下反应,反应达到平衡时的温度与压强的关系如下
| 剩余压强mmHg | 760 | 10 | 1 | 0.1 |
| 平衡时的温度℃ | 2370 | 1700 | 1430 | 1235 |
防止高温下Mg被空气氧化
防止高温下Mg被空气氧化
②降低反应所需温度,节约能源
降低反应所需温度,节约能源
(4)含镁矿物常见的有菱镁矿(MgCO3)、白云石和光卤石(KCl?MgCl2?6H2O),其中
KCl?MgCl2?6H2O属于
A
A
.A.盐 B.混合物
(5)写出煅烧白云石的反应化学方程式
CaCO3?MgCO3
CaO?MgO+2CO2↑
| ||
CaCO3?MgCO3
CaO?MgO+2CO2↑
.
| ||
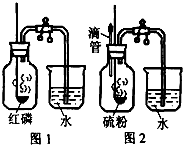 “空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶内气体冷却至室温时,打开止水夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶内气体冷却至室温时,打开止水夹,水注入集气瓶.回答下列问题:(1)反应结束后,打开止水夹,水自动注入集气瓶,约占瓶内总体积的
| 1 |
| 5 |
| 1 |
| 5 |
(2)乙生也设计了一个如图2所示的实验方案,同甲类似,只不过用硫粉代替了红磷,并增加了滴管(其中装有氢氧化钠溶液,氢氧化钠可以与二氧化硫反应).点燃硫粉,看到
淡蓝
淡蓝
色的火焰,待硫熄灭并冷却后滴入液体并打开止水夹,水会
会
(填“会”或“不会”)倒吸,原因是生成的二氧化硫与氢氧化钠反应使瓶内压强变小
生成的二氧化硫与氢氧化钠反应使瓶内压强变小
.(3)若空气中氮气也能和红磷反应,能否用该方法来测定空气中氧气的含量?
不能
不能
.