摘要: Na2CO3和CuSO4等物质.在从水溶液中析出时.常会带出一部分水分子.上述两种物质形成的结晶水合物的化学式分别为 . .
网址:http://m.1010jiajiao.com/timu3_id_116352[举报]
(1)根据下表要求,把水污染情况及防治建议填写在表中.
(2)水既是一种重要的反应物,也是许多化学反应中的生成物.如:化合反应 H2O+CaO=Ca(OH)2.请按照要求写出符合下列反应类型的化学方程式:
分解反应(水是反应物) ,
复分解反应(水是生成物) .
(3)某学习小组采集了从秦淮河的源头到三汊河入江口各段水样.发现有部分水段的水质较差,并对水样进行以下实验检测:
若水样中可能含有CuSO4、FeCl3、Na2CO3、MgCl2、NaCl、H2SO4中一种或几种,试根据实验分析水样中一定不含有的物质是 ;
一定含有的物质是 ;不一定含有的物质是 .
(4)很多地区冬天下大雪,为防止路面结冰,人们往往在路面上撒些食盐.
我们知道纯水结成冰的温度为0℃(冰的熔点).请你设计一个实验来证明食盐对降低水的凝固点的作用.
查看习题详情和答案>>
| 污染分类 | 污染现象 | 污染源 | 防止建议 |
| 生活污染 | 垃圾、生活废弃物等 | ||
| 工业污染 | 流淌黄色液体 | 化工厂废水 | 废水必须经过处理后才能排放 |
| 农业污染 | 农药流入湖中 |
分解反应(水是反应物)
复分解反应(水是生成物)
(3)某学习小组采集了从秦淮河的源头到三汊河入江口各段水样.发现有部分水段的水质较差,并对水样进行以下实验检测:
| 实验内容和步骤 | 实验现象 |
| ①观察水样 | 浅黄色 |
| ②取少量水样,用pH试纸检测 | pH=3 |
| ③另取少量水样,向其中滴加过量氢氧化钠溶液 | 无白色沉淀产生 |
| ④取步骤③中的溶液,滴加过量的稀硝酸和硝酸钡溶液 | 有白色沉淀产生 |
一定含有的物质是
(4)很多地区冬天下大雪,为防止路面结冰,人们往往在路面上撒些食盐.
我们知道纯水结成冰的温度为0℃(冰的熔点).请你设计一个实验来证明食盐对降低水的凝固点的作用.
| 实验设计 | 设计意图 |
| 1、在试管中加入水,插入温度计,冷冻,测量结冰时的凝固点 | |
| 2、 |
|
(1)根据下表要求,把水污染情况及防治建议填写在表中.
| 污染分类 | 污染现象 | 污染源 | 防止建议 |
| 生活污染 | ______ | 垃圾、生活废弃物等 | ______ |
| 工业污染 | 流淌黄色液体 | 化工厂废水 | 废水必须经过处理后才能排放 |
| 农业污染 | ______ | 农药流入湖中 | ______ |
分解反应(水是反应物)______,
复分解反应(水是生成物)______.
(3)某学习小组采集了从秦淮河的源头到三汊河入江口各段水样.发现有部分水段的水质较差,并对水样进行以下实验检测:
| 实验内容和步骤 | 实验现象 |
| ①观察水样 | 浅黄色 |
| ②取少量水样,用pH试纸检测 | pH=3 |
| ③另取少量水样,向其中滴加过量氢氧化钠溶液 | 无白色沉淀产生 |
| ④取步骤③中的溶液,滴加过量的稀硝酸和硝酸钡溶液 | 有白色沉淀产生 |
一定含有的物质是______;不一定含有的物质是______.
(4)很多地区冬天下大雪,为防止路面结冰,人们往往在路面上撒些食盐.
我们知道纯水结成冰的温度为0℃(冰的熔点).请你设计一个实验来证明食盐对降低水的凝固点的作用.
| 实验设计 | 设计意图 |
| 1、在试管中加入水,插入温度计,冷冻,测量结冰时的凝固点 | ______ |
| 2、 ______ | ______ |
(1)根据下表要求,把水污染情况及防治建议填写在表中.
(2)水既是一种重要的反应物,也是许多化学反应中的生成物.如:化合反应 H2O+CaO=Ca(OH)2.请按照要求写出符合下列反应类型的化学方程式:
分解反应(水是反应物)______,
复分解反应(水是生成物)______.
(3)某学习小组采集了从秦淮河的源头到三汊河入江口各段水样.发现有部分水段的水质较差,并对水样进行以下实验检测:
若水样中可能含有CuSO4、FeCl3、Na2CO3、MgCl2、NaCl、H2SO4中一种或几种,试根据实验分析水样中一定不含有的物质是______;
一定含有的物质是______;不一定含有的物质是______.
(4)很多地区冬天下大雪,为防止路面结冰,人们往往在路面上撒些食盐.
我们知道纯水结成冰的温度为0℃(冰的熔点).请你设计一个实验来证明食盐对降低水的凝固点的作用.
查看习题详情和答案>>
| 污染分类 | 污染现象 | 污染源 | 防止建议 |
| 生活污染 | ______ | 垃圾、生活废弃物等 | ______ |
| 工业污染 | 流淌黄色液体 | 化工厂废水 | 废水必须经过处理后才能排放 |
| 农业污染 | ______ | 农药流入湖中 | ______ |
分解反应(水是反应物)______,
复分解反应(水是生成物)______.
(3)某学习小组采集了从秦淮河的源头到三汊河入江口各段水样.发现有部分水段的水质较差,并对水样进行以下实验检测:
| 实验内容和步骤 | 实验现象 |
| ①观察水样 | 浅黄色 |
| ②取少量水样,用pH试纸检测 | pH=3 |
| ③另取少量水样,向其中滴加过量氢氧化钠溶液 | 无白色沉淀产生 |
| ④取步骤③中的溶液,滴加过量的稀硝酸和硝酸钡溶液 | 有白色沉淀产生 |
一定含有的物质是______;不一定含有的物质是______.
(4)很多地区冬天下大雪,为防止路面结冰,人们往往在路面上撒些食盐.
我们知道纯水结成冰的温度为0℃(冰的熔点).请你设计一个实验来证明食盐对降低水的凝固点的作用.
| 实验设计 | 设计意图 |
| 1、在试管中加入水,插入温度计,冷冻,测量结冰时的凝固点 | ______ |
| 2、 ______ |
______ |
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是________.
(2)称取10.6 g该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到的数据如下表:
计算该样品中Na2CO3的质量分数.
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是________.

(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量________变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
废液中的溶质是什么
盐酸和硫酸是两种常见的、重要的酸,在水溶液中都能解离出H+,它们有许多相似的化学性质.熟练掌握稀盐酸、稀硫酸的化学性质可顺利解答有关酸的探究题.
(2013?海安县模拟)(1)根据下图回答问题:
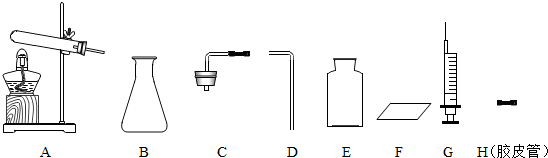
①小东同学选择上图中的B、C、D、E、F仪器制取氧气,则化学反应原理为
②小东在实验前先连接B、C仪器,然后将注射器G与C的胶皮管相连,再向外拉动注射器的活塞一段距离后松开活塞,发现注射器的活塞能回到原来的位置.他进行该步操作的目的是
③小明想利用反应2NaHCO3
Na2CO3+H2O+CO2↑制取少量二氧化碳气体,你认为他应该选择上图中的
(2)某实验小组的同学在加热铜与浓硫酸的混合物实验时,发现生成了一种无色有刺激性气味的气体和蓝色溶液,进行如下探究活动.
[查阅资料]①铜能与一些强氧化性的酸(如浓硫酸、硝酸等)发生反应,生成水、气体和铜盐.②硫酸铜溶液呈酸性.③二氧化硫与高锰酸钾溶液反应并使其褪色.
[探究一]铜与浓硫酸反应生成的气体是什么?
[猜想分析]小兰认为生成的气体可能是氢气或氧气.小芳马上予以否定,她的理由是
[实验论证]她们将生成的气体通入稀的高锰酸钾溶液,看到
[探究二]铜与浓硫酸反应得到的蓝色溶液是什么?
[分析讨论]①对于生成的蓝色溶液,小强认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而可能是硫酸铜溶液,小楠的理由是
②根据分析写出铜与浓硫酸共热的化学方程式
③小吉根据化学方程式说,该方法适用于以铜为原料大量制取硫酸铜,小田认为不适宜,你能说出小田的一个理由吗
[探究三]上述反应后的蓝色溶液中有硫酸剩余吗?
[实验讨论]①小伟认为可向蓝色溶液中滴加硝酸钡溶液,观察有无沉淀产生,经大家讨论后,该方案被否定,你觉得否定该方案的理由是
②小亮同学提问:可以用石蕊试液来进行检验吗?你的答案和理由是
[意外发现]实验小组的同学将足量的铜和足量的浓硫酸置于容器中加热一段时间后,发现反应会逐渐变慢,最后反应竟然停止,你能帮他们说出反应停止的原因吗?
查看习题详情和答案>>

①小东同学选择上图中的B、C、D、E、F仪器制取氧气,则化学反应原理为
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
(用化学方程式表示)
| ||
②小东在实验前先连接B、C仪器,然后将注射器G与C的胶皮管相连,再向外拉动注射器的活塞一段距离后松开活塞,发现注射器的活塞能回到原来的位置.他进行该步操作的目的是
检查装置的气密性
检查装置的气密性
.③小明想利用反应2NaHCO3
| ||
ADEF
ADEF
(填仪器或装置的序号)组装一套发生和收集装置.(2)某实验小组的同学在加热铜与浓硫酸的混合物实验时,发现生成了一种无色有刺激性气味的气体和蓝色溶液,进行如下探究活动.
[查阅资料]①铜能与一些强氧化性的酸(如浓硫酸、硝酸等)发生反应,生成水、气体和铜盐.②硫酸铜溶液呈酸性.③二氧化硫与高锰酸钾溶液反应并使其褪色.
[探究一]铜与浓硫酸反应生成的气体是什么?
[猜想分析]小兰认为生成的气体可能是氢气或氧气.小芳马上予以否定,她的理由是
氢气或氧气是无色无味的气体
氢气或氧气是无色无味的气体
.经过仔细分析,她们认为该气体可能是二氧化硫.[实验论证]她们将生成的气体通入稀的高锰酸钾溶液,看到
高锰酸钾溶液褪色
高锰酸钾溶液褪色
现象,从而证实了生成的气体是二氧化硫.[探究二]铜与浓硫酸反应得到的蓝色溶液是什么?
[分析讨论]①对于生成的蓝色溶液,小强认为可能是Cu(NO3)2溶液,小楠认为不可能是Cu(NO3)2溶液,而可能是硫酸铜溶液,小楠的理由是
反应前后元素的种类不变
反应前后元素的种类不变
.②根据分析写出铜与浓硫酸共热的化学方程式
Cu+2H2SO4
CuSO4+2H2O+SO2↑
| ||
Cu+2H2SO4
CuSO4+2H2O+SO2↑
.
| ||
③小吉根据化学方程式说,该方法适用于以铜为原料大量制取硫酸铜,小田认为不适宜,你能说出小田的一个理由吗
生成的二氧化硫会污染环境
生成的二氧化硫会污染环境
.小田还设计了一个以铜和稀硫酸为原料制取硫酸铜的更好方案,该方案是铜和氧气反应生成氧化铜,然后将氧化铜与稀硫酸反应得到硫酸铜
铜和氧气反应生成氧化铜,然后将氧化铜与稀硫酸反应得到硫酸铜
.[探究三]上述反应后的蓝色溶液中有硫酸剩余吗?
[实验讨论]①小伟认为可向蓝色溶液中滴加硝酸钡溶液,观察有无沉淀产生,经大家讨论后,该方案被否定,你觉得否定该方案的理由是
硫酸铜中也含有硫酸根离子,也能和氯化钡溶液反应生成白色沉淀
硫酸铜中也含有硫酸根离子,也能和氯化钡溶液反应生成白色沉淀
.②小亮同学提问:可以用石蕊试液来进行检验吗?你的答案和理由是
不可以;因为硫酸铜溶液也是酸性的,也能使石蕊变红
不可以;因为硫酸铜溶液也是酸性的,也能使石蕊变红
.[意外发现]实验小组的同学将足量的铜和足量的浓硫酸置于容器中加热一段时间后,发现反应会逐渐变慢,最后反应竟然停止,你能帮他们说出反应停止的原因吗?
随着反应的进行,浓硫酸中溶质的质量分数逐渐变小,稀硫酸与铜不反应
随着反应的进行,浓硫酸中溶质的质量分数逐渐变小,稀硫酸与铜不反应
.