摘要:在两个小烧杯中分别装入10MLH+浓度为3G/L和稀盐酸和稀硫酸.向两烧杯中各加入大小为0.1*10*25MM纯度≥99.5%的铝片.实验现象记录如下: 反应时间 1 2 5 15 20 反应现象 稀盐酸 少量气泡 较多气泡 大量气泡 反应剧烈 铝片耗尽 稀硫酸 无明显现象 提出问题:溪盐酸和稀硫酸都是非金属氧化物.在水溶液里均能电离出H+.大小.纯度完全相同的铝片与H+浓度相同的两种稀酸反应.理论上反应速率应该相等.而实际上铝片稀盐酸反应剧烈.与稀硫酸几乎不反应.是什么原因引起的呢? 根据小表要求.填写表中空格. 作出假设 实验探究 1 Cl-能促进铝片与H+反应 2
网址:http://m.1010jiajiao.com/timu3_id_109502[举报]
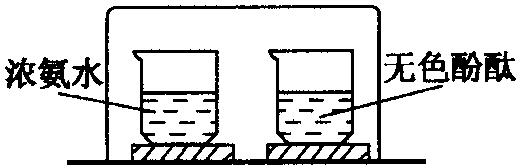
已知浓氨水具有挥发性,挥发出的氨气又极易溶于水,氨水具有碱性可以使无色酚酞试液变红色。
某学生做实验如下:在两个小烧杯中分别盛有无色浓氨水和无色酚酞试液,把两个小烧杯放在一个倒扣的大烧杯中,如下图所示。
问题:
①过一段时间后,会有什么现象发生________
②此实验说明了分子________,浓氨水的物理性质有________,化学性质有________。
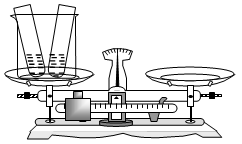
查看习题详情和答案>> (2012?天桥区三模)为了验证质量守恒定律,在两个小试管中分别注入20g 4.9%稀硫酸和20g氯化钡溶液,放于一个大烧杯中称量,如图所示.试根据要求,回答下列问题:
(2012?天桥区三模)为了验证质量守恒定律,在两个小试管中分别注入20g 4.9%稀硫酸和20g氯化钡溶液,放于一个大烧杯中称量,如图所示.试根据要求,回答下列问题:(1)将两只小试管内药品充分混合后,写出观察到的一项实验现象:
有白色沉淀生成
有白色沉淀生成
.(2)混合后,反应结束后,整个装置的质量与之前相此较
①
①
(填写下列各项的序号). ①没有变化 ②有变化,后者质量变小 ③有变化,后者质量变大 ④不能确定
(3)若稀硫酸完全反应,试通过计算,求此时所得不饱和溶液的质量.(写出相应计算过程,计算结果精确至0.01g)
(7分)为了验证质量守恒定律,在两个小试管中分别注入20g4.9%稀硫酸和20g氯化钡溶液,放于一个大烧杯中称量,如图所示
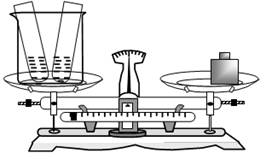
试根据要求,回答下列问题:
(1)将两只小试管内药品充分混合后,写出观察到的一项实验现象: 。
(2)混合后,反应结束后,整个装置的质量与之前相此较_______(填写下列各项的序号)。 ①没有变化 ②有变化,后者质量变小 ③有变化,后者质量变大 ④不能确定
(3)若稀硫酸完全反应,试通过计算,求此时所得不饱和溶液的质量。(写出相应计算过程,计算结果精确至0.01g)
查看习题详情和答案>>