摘要:(三)链接中考与竞赛 1.长期存放石灰水的试剂瓶内壁常附有一层白色固体.要洗去这层白色固体最好的方法是 A.用水洗 B.用氢氧化钠溶液洗 C.用盐酸洗 D.先用盐酸荡洗再用水冲洗 2.为探究植物光合作用的实质.某校学生设计了如下实验装置.在阳光下.你预测数天后植物生长最茂盛的是( ) 3.即食即热型快餐的内层是用铝箔真空包装的食物.外层则分别包装两包物质.使用时拉动预留在外的拉线.使这两种物质反应.便可对食物进行加热.这两包物质最适合的选择是 ( ) A.浓硫酸与水 B.生石灰与水 C.熟石灰与水 D.氯化钠与水 4.如图所示.一个广口瓶中放一只健康的小白鼠,另一个广口瓶中放一小烧杯.烧杯中盛有足量的浓NaOH溶液.并漂浮着一个小球(小球不与其他物质反应.实验装置足以维持小白鼠的生命活动.忽略水蒸气.温度.压强变化对实验的影响).数小时后小球会( ) A.上浮一些 B.下沉一些 C.仍在原处 D.沉到杯底 5.为了检验长期暴露在空气中的氢氧化钠溶液是否变质.可选择三种不同类别的物质进行实验.请你写出所选试剂的化学式:酸 .碱 .盐 . 6.为证明二氧化碳与氢氧化钠发生了化学反应.小明进行实验后的实验报告如下: 实验步骤 实验现象 结论 ①将二氧化碳通入氢氧化钠溶液 无明显现象 由第②步反应生成的碳酸钙.说明反应①有碳酸盐新物质生成.证明发生了化学反应. ②取上述实验所得溶液于试管中.滴入氯化钙溶液. 有白色沉淀生成 ③往白色沉淀中滴入稀盐酸 白色沉淀溶解.有气泡产生 请回答下列问题: (1)写出第①步反应的化学方程式: (2)写出第③步反应的化学方程式: (3)请分析本实验方案的不足之处: (4)还有的同学认为只用空矿泉水瓶就可证明这个是否发生.他的实验方法和现象 . 7.对牙膏有关问题的探究:对牙膏的探究要用到许多化学知识. (1)下表列出了三种牙膏中的摩擦剂.请在表中填写三种摩擦剂所属的物质类别. 两面针儿童牙膏 珍珠王防臭牙膏 中华透明牙膏 摩擦剂 氢氧化铝 碳酸钙 二氧化硅 摩擦剂的物质类别 (2)根据你的推测.牙膏摩擦剂的溶解性是 . (3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备.某学生设计了一种制备碳酸钙的实验方案.其流程图为: 请写出上述方案中有关反应的化学方程式: ① ② ③ (4)请你仍用石灰石为原料.设计另一种制备碳酸钙的实验方案.仿照(3)所示.将你的实验方案用流程图表示出来: 你设计的方案优点是 . (5)检验牙膏中是否含有碳酸盐的实验方法是 . (6)某学生为了测定一种以碳酸钙为摩擦剂的牙膏中碳酸钙的含量.用烧杯称取这种牙膏膏体100.0 g.向烧杯中逐渐加入稀盐酸至不再有气体放出(除碳酸钙外.这种牙膏中的其他物质不能与盐酸反应生成气体).共用去稀盐酸200.0 g.反应完毕后称得烧杯内物质的质量为278.0 g.(所有质量数据均不含烧杯质量)请你计算这种牙膏中碳酸钙的质量分数.(可能用到的相对原子质量:H-1,C-12,O-16,C1-35.5,Ca-40) 课时2 酸和碱之间会发生什么反应
网址:http://m.1010jiajiao.com/timu3_id_103649[举报]
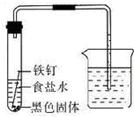 13、某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
13、某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.观察现象:①装置中右侧导管中的液面升高.
②铁钉生锈,试管底部有黑色固体物质.
提出问题:导管中液体为何升高?黑色固体物质又是什么?
理论分析:小组同学根据已学过的知识分析得知,液面上升的原因是
铁钉生锈消耗了试管内的氧气,使试管内压强低于大气压.(合理即可)
.[猜想与假设]小组中的小明同学猜测该黑色固体可能含有:
①Fe、②Fe2O3、③FeCl3、④C四种物质.
[分析与验证]小组同学根据小明的四种猜测做了以下分析:
(1)小红同学认为不可能含有氯化铁,该结论得到小组同学的认可,理由是
氯化铁溶于水
.(2)小强同学认为一定含有碳,该结论也得到小组同学的认可,理由是
铁钉是铁合金,含有碳
.(3)小组同学不能确定是否含有铁,请人帮他们设计方案进行确认:
| 实验步骤 | 实验现象 | 实验结论 |
稀盐酸(或稀硫酸) |
有气泡产生(无气泡产生) |
含有(或不含有) |
食盐水
(填“水”或“食盐水”)中生锈快.29日晚6时许,京沪高速淮安段,一辆槽罐车与一辆迎面驶来的解放牌大货车相撞后翻倒在地,槽罐车司机逃逸,槽罐车上满载的约32吨液态氯气快速泄漏.与事故发生地相距300米的地方,是一个村庄,住有l万名村民.到3月30日下午5时,中毒死亡者达27人,送医院治疗285人.
相关链接:氯气为黄绿色气体,有强烈刺激性气味,在常温下,l体积的水能溶解2体积的氯气,氯气密度为3.21g/L(空气为1.293g/L),高压下可呈液态,氯气与碱反应生成次氯酸盐(CIO-为次氯酸根)和金属氯化物等.据专家介绍,氯气被人吸入后,可迅速附着于呼吸道黏膜,之后可以导致人体支气管痉挛、支气管炎、支气管周围水肿、充血和坏死.呼吸道黏膜受刺激,可造成局部平滑肌痉挛,再加上黏膜充血、水肿及灼伤,可引起严重的通气障碍.人吸入的浓度为每立方米2.5mg的氯气时,就会死亡.
回答下列问题
(1)氯气的物理性质是:
(2)氯气的化学性质是:
(3)为什么储氯罐内温度升高会引起爆炸?(用分子的观点说明)
(4)储氯罐发生的爆炸是物理变化,还是化学变化?为什么?
(5)根据储氯罐发生泄漏时的实际状况请回答:你如何迅速、安全地逃离事故现场?
(6)氯气泄漏发生后,一直在现场待命的消防特勤队立即用高压水网(火碱液NaOH)连续高空稀释,在较短时间内有效控制了氯气扩散.请写出该反映的化学方程式:
查看习题详情和答案>>
相关链接:氯气为黄绿色气体,有强烈刺激性气味,在常温下,l体积的水能溶解2体积的氯气,氯气密度为3.21g/L(空气为1.293g/L),高压下可呈液态,氯气与碱反应生成次氯酸盐(CIO-为次氯酸根)和金属氯化物等.据专家介绍,氯气被人吸入后,可迅速附着于呼吸道黏膜,之后可以导致人体支气管痉挛、支气管炎、支气管周围水肿、充血和坏死.呼吸道黏膜受刺激,可造成局部平滑肌痉挛,再加上黏膜充血、水肿及灼伤,可引起严重的通气障碍.人吸入的浓度为每立方米2.5mg的氯气时,就会死亡.
回答下列问题
(1)氯气的物理性质是:
常温下,氯气为黄绿色气体,有刺激性气味,能溶于水,密度为3.21g/L.
常温下,氯气为黄绿色气体,有刺激性气味,能溶于水,密度为3.21g/L.
;(2)氯气的化学性质是:
氯气与碱反应生成次氯酸盐和金属氯化物
氯气与碱反应生成次氯酸盐和金属氯化物
;(3)为什么储氯罐内温度升高会引起爆炸?(用分子的观点说明)
(4)储氯罐发生的爆炸是物理变化,还是化学变化?为什么?
(5)根据储氯罐发生泄漏时的实际状况请回答:你如何迅速、安全地逃离事故现场?
(6)氯气泄漏发生后,一直在现场待命的消防特勤队立即用高压水网(火碱液NaOH)连续高空稀释,在较短时间内有效控制了氯气扩散.请写出该反映的化学方程式:
2NaOH+Cl2=NaCl+NaClO+H2O
2NaOH+Cl2=NaCl+NaClO+H2O
.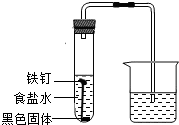 某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.观察现象:
①装置中右侧导管中的液面升高.
②铁钉生锈,试管底部有黑色固体物质.
提出问题:导管中液体为何升高?黑色固体物质又是什么?
理论分析:小组同学根据已学过的知识分析得知,液面上升的原因是
猜想与假设:小组中的小明同学猜测该黑色固体可能含有:①
分析与验证:小组同学根据小明的四种猜测做了以下分析:
(1)小红同学认为不可能含有氯化铁,该结论得到小组同学的认可,理由是
(2)小强同学想证明是否含有碳,他设计了下列方案并进行实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取少量黑色固体,滴加足量稀盐酸一定含有碳 |
| 实验步骤 | 实验现象 | 实验结论 |
| 你选用的试剂是: |
反思:防止铁制品生锈的方法是
 (2007?常州)新闻链接:2005年3月19日,某校3位学生在实验操作中不慎将钠与水接触,引发火灾…
(2007?常州)新闻链接:2005年3月19日,某校3位学生在实验操作中不慎将钠与水接触,引发火灾…阅读了上述新闻之后,好奇的唐唐猜测:金属钠能与水发生反应.
她通过查找资料获得了以下信息:
①钠常温下在空气中易氧化成氧化钠(Na2O),氧化钠可与水化合生成相应的碱;
②钠能与水剧烈反应,放出大量的热,化学方程式为:2Na+2H2O=2NaOH+H2↑.
她在老师的指导下设计并进行了实验,并做了如下实验记录:
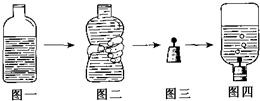
①取一空矿泉水瓶,加入纯净水,仅留一小段空隙,如图一所示;
②用手挤压矿泉水瓶,除去里面的空气,如图二所示;
③在胶塞上固定一根大头针,用针扎起一块金属钠,如图三所示;
④迅速用胶塞塞住挤瘪的瓶口,倒置,如图四所示;
⑤待完全反应后,打开瓶塞,检验产生的气体;
⑥在矿泉水瓶中滴入数滴A试剂,溶液呈红色.
请根据唐唐的实验过程与实验记录,回答以下问题:
(1)写出试剂A的名称:
酚酞
酚酞
;(2)写出氧化钠与水反应的化学方程式:
Na2O+H2O=2NaOH
Na2O+H2O=2NaOH
;(3)为什么在实验步骤②中要除去矿泉水瓶中的空气?
得到纯净的气体,以检验气体,同时避免在检验或反应中发生爆炸
得到纯净的气体,以检验气体,同时避免在检验或反应中发生爆炸
;(4)本实验中,对取用的金属钠的大小是否有要求,为什么?
有要求,黄豆粒大小即可.若金属钠太大,反应很剧烈,不易控制,且生成的气体过多,瓶内压强增大瓶塞可能会顶飞,使实验失败;若金属钠太小,生成的气体过少,反应现象不明显,导致后续实验无法进行
有要求,黄豆粒大小即可.若金属钠太大,反应很剧烈,不易控制,且生成的气体过多,瓶内压强增大瓶塞可能会顶飞,使实验失败;若金属钠太小,生成的气体过少,反应现象不明显,导致后续实验无法进行
.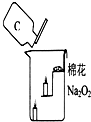 过氧化钠是一种黄色固体,化学式为Na2O2,化学兴趣小组的同学将包有过氧化钠固体的棉花放入如图所示的烧杯中,缓慢倒入二氧化碳气体后,发现位于下面的蜡烛先熄灭,上面的后熄灭,同时发现棉花燃烧起来.
过氧化钠是一种黄色固体,化学式为Na2O2,化学兴趣小组的同学将包有过氧化钠固体的棉花放入如图所示的烧杯中,缓慢倒入二氧化碳气体后,发现位于下面的蜡烛先熄灭,上面的后熄灭,同时发现棉花燃烧起来.(1)实验中:位于下面的蜡烛先熄灭,上面的后熄灭.这一现象说明二氧化碳具有
(2)棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件,还需要满足的条件是
提出问题:在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下Na2O2和CO2能发生化学反应.
设计实验:经过讨论后,小组同学利用如图所示的实验装置进行探究.要使Na2O2与CO2反应,实验装置中导管口正确的链接顺序是
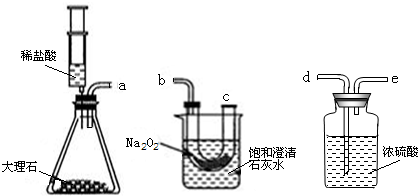
实验步骤:①按以上顺序装好装置,并检查其气密性,添加药品;
②推动注射器,并将稀盐酸注入锥形瓶中;
③一段时间后,在尾气处放置一根带火星的小木条,观察现象.
实验现象:带火星的小木条复燃且饱和澄清石灰水变浑浊.
实验分析:①浓硫酸的作用是
②烧杯内变浑浊的原因是
实验结论;①“小木条复燃”说明了Na2O2和CO2反应产生了
②“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应
(3)已知Na2O2和CO2反应生成上述气体的同时还有纯碱生成.若实验结束后,U型管的质量增加了1.2g,求生成氧气的质量. 查看习题详情和答案>>