2009年辽宁中考综合复习训练化学试题(十)
理化考试时间l50分钟 化学试卷满分65分
可用到的相对原子质量:H―l O―16 Na―
一、选择题(本题包括13道小题,l―11小题每小题1分;l2、13小题每小题2分;共15分,每小题有一个最符合题目要求的选项,请选出后将其序号填在题后的括号内)
1.目前,下列化学制品在生活中不准使用的是 ( )
A.含磷洗衣粉 B.可降解塑料袋 C.高效低毒蚊香 D.合成纤维衣服
2.化学的学习需要一丝不苟的态度,很多基础知识必须搞清楚,请你判断下列说法正确的是 ( )
A.原子中的核外电子离核越近,能量越高
B.pH=5.6的碳酸溶液的酸性大于pH=6.2的硫酸溶液的酸性
C.实验室收集密度比空气小的气体只能用向下排空气集气法
D.除去CO中的较多的CO2,最好的方法是通入澄清石灰水
3.夏日里想随时喝到凉爽的饮料,可以自制化学“冰箱”,即把一种化学试剂放入一定量的水中,就可以形成低温小环境。这种试剂可以是下列物质中的 ( )
A.食盐 B.硝酸铵 C.蔗糖 D.熟石灰
4.欲确保含有盐酸的氯化钙溶液被中和至中性,在不用指示剂的条件下,应加入的试剂是 ( )
A.生石灰 B.熟石灰 C.石灰石粉末 D.纯碱
5.臭氧层是地球的保护伞,超音速飞机的尾气(主要成分NO气体)破坏臭氧层时会发生O3+NO==NO2+O2的反应,该反应中的氧化剂是 ( )
A.O3 B.NO C.NO2 D.O2
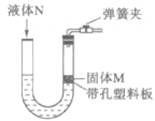
6.下图所示装置可用于实验室制取某些气体,并能随开随用,随关随停。下表中所选用的药品及制取的气体你认为完全正确的一组 ( )
选项
选用的药品
制取的气体
固体N
液体N
A
大理石
稀硫酸
二氧化碳
B
锌粒
浓硫酸
氢气
C
大理石
稀盐酸
二氧化碳
D
碳酸钠
稀硫酸
二氧化碳
7.据华商晨报报导,一辆满载浓硫酸的槽罐车在某路段上因车祸翻倒,浓硫酸大量泄漏,为了不污染旁边的水源,你认为消防队应采取的措施最适宜的是 ( )
A.用水冲洗泄漏的浓硫酸 B.将熟石灰撒在泄漏出的浓硫酸上
C.将氯化钡撒在泄漏出的浓硫酸上 D.用土将泄漏出的浓硫酸掩埋
8.La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3,难溶于水,而LaCl3、La(NO3)3都易溶于水。下列各组物质中,不能直接反应生成LaCl3的是 ( )
A.La+HCl B.La2O3+HCl C.La(OH)3+HCl D.BaCl2+La(NO3)3
9.现有三种常见治疗胃病药品的标签:

药品中所含的物质均能中和胃里过量的盐酸,下列关于三种药片中和胃酸的能力比较,正确的是 ( )
A.①=②=③ B.①>②>③ C.③>②>① D.②>③>①
10.在实验室里,某同学想用实验证明硫酸铜溶液显蓝色与SO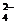 无关,你认为该同学进行下列实验无意义的是 ( )
无关,你认为该同学进行下列实验无意义的是 ( )
A.观察硫酸钠溶液没有颜色
B.向硫酸铜溶液中滴加适量的氯化钡溶液,振荡后静置,溶液蓝色未消失
C.向硫酸铜溶液中滴加适量的氢氧化钠溶液,振荡后静置,溶液蓝色消失
D.加水稀释硫酸铜溶液,溶液蓝色变浅
11.某工厂废液中含有少量硫酸,拟选用下列物质中和后再排放:
物质
CaCO3
Ca(OH)2
NH3
NaOH
市场参考价
1.8
2.0
6.5
11.5
如果要求花最少的钱来中和相同量的废硫酸,则应选择 ( )
A.CaCO3 B.Ca(OH)
12.如图是他们设计的一个二氧化碳发生装置,对其优缺点的评价,错误的是 ( )
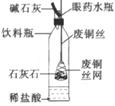
A.所用材料均为家庭废品,有较好的资源利用意识
B.使用碱石灰(只要成分NaOH和生石灰)有利于得到干燥的二氧化碳气体
C.将石灰石放入铁丝网,不用时可向上拉动铜丝,使反应中止,与酸接触后又不与酸反应,体现便利使用的设计思想
D.利用拉动铜丝的设计,要注意保证气密性良好,方能使实验成功
13.烧杯中盛满一定浓度的醋酸溶液(溶液密度约为
A.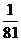 B.
B.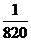 C.
C.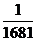 D.无法确定
D.无法确定
二、填空题(本题包括4道小题,每空1分,共14分)
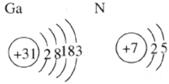
14.纳米技术的研究是当前世界科技研究的一个热点,1998年中国科学家合成了纳米氮化镓,已知镓(Ga)和氮的原子结构示意图:则氮化镓的化学式最可能是: ______。
15.已知明矾是一种良好的净水剂,可用于家庭饮用水的净化,它的化学式:
KAl(SO4)2?12H2O,明矾溶于水后全部电离为K+、Al3+和SO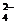 ,请回答下列问题:
,请回答下列问题:
(1)明矾水溶液的导电性_________(填“良好”或“差”)
(2)往明矾水溶液中滴加几滴氯化镁溶液,是否有明显现象出现__________;
(3)已知K2SO4溶液,KCl溶液的PH=7,AlCl3溶液、Al2(SO4)3溶液的pH<7。
请猜想用明矾净化后的水,其pH________(填“>”、“<”或“=”)7。
16.俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形。下表为元素周期表的部分示意图,表中数字为各元素原子的质子数。
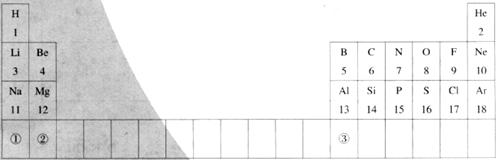
(1)用符号表示:带两个单位负电荷且质子数为8的离子__________(写一种),AB2型化合物_________(写一种);
(2)去年底重庆开县发生天然气“井喷”事件。喷出的气体中有一种有毒的含有18个质子的A2B型气体,其水溶液是一种无氧酸,请用符号和数字表示:3个A2B分子__________;
(3)研究表中各元素原子的质子数,可发现元素从左向右的排列规律是__________,请预测质子数为20的元素在表中的位置_______________(填①、②、③)。该元素离子的结构示意图是__________。(填“甲”或“乙”)

17.维生素C(C2H8O6)又叫抗坏血酸。1907年挪威化学家霍尔斯特在柠檬汁中发现,现已人工合成。维生素C主要存在于蔬菜、水果中。它是无色晶体,易溶于水,水溶液呈酸性。它的化学性质较活泼,遇热、碱和重金属离子容易分解,人体长期缺少维生素C会得坏血病。据诺贝尔奖获得者鲍林研究,服用维生素 对预防感冒和抗癌有一定作用。
试回答:
(1)每个维生素C分子共有________个原子;
(2)维生素C的相对分子质量为________,各元素的质量比C:H:O=__________;
(3)写出维生素C的物理性质或化学性质(只写一种即可):
______________________________________________________________________。
三、简答题(本题包括5道小题,共22分)
18.(分)举例来证明下列结论是错误的:
(1)有盐和水生成的反应一定是中和反应;
(2)物质的溶解度随着温度的升高都会增大;
(3)原子团在化学反应中都作为一个整体参加反应,一定不发生变化。
19.(6分)某电镀厂排放的废水含有大量有毒重金属盐Ba(NO3)2、Cu(NO3)2、AgNO3,该厂想用氢氧化钾溶液、盐酸、硫酸三种试剂,将所排废水中的重金属离子逐一变成沉淀回收,最后得到只含一种化肥的中性溶液。假设每种试剂只用一次,每步恰好完全反应。请你按照所加试剂的顺序,写出生成三种沉淀的化学方程式:
第一步___________________________________________________________________;
第二步___________________________________________________________________;
第三步___________________________________________________________________。
20.(3分)当电器设备失火时,你认为在酸碱灭火器、泡沫灭火器和液态二氧化碳灭火器中应选择哪种灭火器?请你谈一谈你选择的原因。
21.(4分)下面是在厦门市鼓浪屿淑庄花园前新设的一组垃圾箱及说明:

厦门市生活垃圾分类种类
可回收垃圾
不可回收垃圾
有害垃圾
1.纸类
2.玻璃
3.金属
4.塑料
5.橡胶
6.纺织品
1.厨房垃圾
2.灰土
3.杂草
4.枯枝
5.花卉
1.日光灯管
2.电池
3.喷雾罐
4.指甲油瓶
5.药品药瓶
6.涂改液瓶
(1)小明在整理房间时,清理出如下物品,它们应分别放入哪个垃圾箱(请填序号);
A.废作业本 B.汽水易拉罐 C.生锈铁钉 D.矿泉水瓶 E.烂苹果F.涂改液瓶
应放入“可回收垃圾箱”的是:_______________________________________________,
应放入“有害垃圾箱”的是:________________________________________________。
(2)请从可回收垃圾的类别中,举出一例说说化学的研究成果给社会进步带来的贡献:
__________________________________________________________________________;
(3)化学电池给人们生活带来许多便利,但任意丢弃的一粒电池将严重污染一平方米土壤。一些化学成就在给人们带来方便的同时,也给人类带来危害。对此,你认为在进行化学科学研究或发明时要注意的是:________________________________________________。
22.(6分)下表是行星上“大气” (相当于地球上的空气)的主要成分。请回答下列问题:

行星名称
行星上“大气”主要成分
金星
二氧化碳、硫酸
火星
二氧化碳
冥王星
甲烷
(1)它们中可能成为宇宙飞船燃料补给站的行星是:___________________________;
(2)科学家发现在宇宙飞船飞过冥王星“大气”时,甲烷并没有被点燃,请分析原因:
_______________________________________________________________________;
(3)上图是我国“长征”系列火箭发射升空的情景,该火箭第一级是用联肼(N2H4)作为燃料,用一氧化氮作为助燃剂,燃烧生成水和空气中最多的气体,请写出该反应的化学方程式:_____________________________________________________________________________;
(4)“勇气”号近日测得温度很高的火星 表层土壤中可溶性盐的含量高,科学家认为这是火星“地下”有水的证据,请结合溶液的有关知识,谈谈为什么把这个发现认为是火星有水的证据:______________________________________________________。科学家让“勇气”号在火星上找水的意义是:___________________________________________________。
(5)若要在月球上建立永久空间站,需要解决空间站内氧气和二氧化碳之间循环的问题,请提出你的一个设想:_________________________________________________________。
四、探究题(本题包括1道小题,共8分)
23.(8分)氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO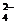 )能使氧化铜溶解。请你和他一起通过下图Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究活动。
)能使氧化铜溶解。请你和他一起通过下图Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究活动。

(1)(1分)你提出的假设是____________________________________;
(2)(2分)通过实验Ⅰ可以证明____________________________________;
(3)(2分)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入_______________________________________________________________________;
(4)(3分)探究结果为_______________________________,你认为除实验Ⅱ和Ⅲ所用试剂外,还能够溶解氧化铜的一种常见物质是_________________________。(此空1分)
五、计算题(本题包括1道小题,共6分)
24.(6分)将
(1)此混合物中硫酸铁为多少克?
(2)反应后溶液的溶质质量分数。(答案精确到小数点后两位)