2008年江苏省启东中学中考模拟考试(十三)
化学试卷
可能用到的相对原子质量:C-12 H一1 O-16 Na-23 Ca-40 Ba-
S-32 Zn-65 Fe-56
一、选择题(本题包括l5小题,每小题2分,共30分。每小题只有一个选项符合题意)
1.现代社会对能量的需求越来越大。图l3-1是利用不同形式的能量发电的示意图,其中属于化学变化的是
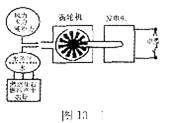
A.燃烧化石燃料产生热量
B.水受热变为水蒸气
C.风力、水力、潮汐力、水蒸气带动涡轮机转动
D.发电机工作产生电能
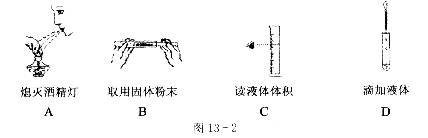
2.图l3-2中的实验操作不正确的是
3.硅(Si)是现代电子工业的基础。工业上制取粗硅的反应原理为:Si O2 + Si+ 2CO,该反应的基本类型是( )
Si+ 2CO,该反应的基本类型是( )
A.分解反应 B.置换反应
C.化合反应 D.复分解反应
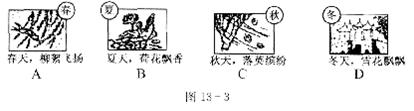
4.“珠帘十里卷春风”、“绿杨城郭是扬州”。来过扬州的人无不为扬州城的美丽风景所吸引。观察图13-3,图中现象能说明分子在不断运动的是 ( )
5.物质X是一种重要的阻燃剂,工业上用三氧化二锑[Sb2O3]生产X的化学方程式为Sb2O3+2 H2O2==X+2 H2O根据质量守恒定律,推断X的化学式为( )
A.SbO2 B.H SbO3
C.Sb2O5 D.H3 SbO4
6.今年世界水日的主题是“应对水短缺”。下列应对水短缺的措施:①推广使用无磷洗衣粉;②加强工业废水的达标排放;③加快生活污水净化处理的建设;④合理使用农药和化肥;⑤提倡节约用水,其中合理的是 ( )
A.①②③ B.①②④⑤ C.②③④⑤ D.①②③④⑤
7.下列叙述错误的是 ( )
A.稀释浓硫酸时将水迅速地倒人盛浓硫酸的烧杯中
B.篝火晚会时通常把木柴架空一些,使燃烧更旺
C.自行车支架上刷上油漆既美观又能防止钢铁生锈
D.利用洗涤剂的乳化功能可洗去餐具上的油污
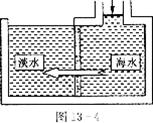
8.海水淡化可采用膜分离技术,如图l34所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水,对加压后右侧海水成分变化进行分析,正确的是 ( )
A.溶质质量增加
B.溶液质量不变
C.溶剂质量减少
D.溶质质量分数不变
9.鉴别日常生活中的下列物品,方法不正确的是 ( )
选项
鉴别的物质
方 法
A
硬水和软水
加肥皂水搅拌,观察产生泡沫的多少
B
食盐和白砂糖
尝味道
C
棉布料和化纤布料
灼烧、闻气味
D
蒸馏水和矿泉水
观察颜色
10.某省一石化公司双苯厂发生爆炸,造成江水污染,主要污染物之一是苯。图l3-5是苯的微观粒子模拟图,请根据图示判断下列说法错误的是 ( )

A.苯的化学式为C6H6 B.苯由两种元素组成
C.苯是由碳原子、氢原子直接构成的 D.苯属于有机化合物
11. 分别表示x、Y、Z三种不同的气体分子,其在一定条件下反应前后的变化如图l3-6所示。下列叙述错误的是 ( )
分别表示x、Y、Z三种不同的气体分子,其在一定条件下反应前后的变化如图l3-6所示。下列叙述错误的是 ( )

A.分子是在不断运动的 B.分子之间是有间隔的
C.该反应可表示为3X+Y=2Z D.一个Z分子由三个原子构成
12.观察和实验是研究化学的基本方法,下列通过实验得出的结论错误的是 ( )
A.铁丝可以在氧气中燃烧,说明氧气具有可燃性
B.金刚石和石墨在氧气中燃烧生成同一种产物,说明金刚石和石墨的组成元素相同
C.用pH试纸检验某工厂排出的废水,结果pH=3,说明废水呈较强的酸性
D.将酚酞试液分别滴人烧碱溶液和石灰水中,溶液均变红,说明碱溶液能使酚酞试液变红
13.缺钙能导致儿童发育不良或佝偻病。小明从食物中摄入钙元素不足,每天还需要服用2片某种钙片。该钙片标签的部分内容如图l3―7所示(钙片中只有碳酸钙含有钙元素),小明每天从钙片中摄入钙元素的质量为 ( )

A.0.
14.下列各组实验,不能说明镁和铜的金属活动性强弱的是 ( )
A.镁条和铜丝分别插入稀硫酸中 B.镁条和铜丝分别插入氢氧化钠溶液中
C.铜丝插入硫酸镁溶液中 D.镁条和铜丝分别在氧气中点燃
15.已知两种分子E和G反应生成另外两种分子L和M(图l3-8)。则下列判断正确的是 ( )

A.G和M是单质 B.L可能是氯化物
C.这是一个复分解反应 D.这是一个是置换反应
二、选择题(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给2分,但只要选错一个,该小题就为0分)
16.实现H2SO4 H2
H2 H2O转化,可能包含的化学反应基本类型是 ( )
H2O转化,可能包含的化学反应基本类型是 ( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
17.取四种植物的花瓣分别放在研钵中,加入酒精研磨,得到花汁。各取少许花汁,用稀酸或稀碱进行检验,结果如下表所示:
花的种类
花汁在酒精中的颜色
花汁在酸溶液中的颜色
花汁在碱溶液中的颜色
大红花
粉红色
橙色
绿色
玫瑰
粉红色
粉红色
绿色
万寿菊
黄色
黄色
黄色
雏菊
无色
无色
黄色
则下列说法不正确的是 ( )
A.研磨花瓣过程中加入酒精是为了溶解其中的色素
B.
C.万寿菊花汁能用作酸碱指示剂
D. 可用雏菊花汁来区别HCl和NaOH溶液
18.下列各组物质的溶液,不另加试剂无法一一鉴别的是 ( )
A.NaOH、HCl、CuSO4、MgSO4 B.Na2CO3、K2SO4、BaCl2、HCl
C.KNO3、HCl、CaCl2、NaOH D.NH4NO3、H2SO4、NaOH、MgCl2
19.把氧化铜和铁粉的混合物加到一定量的盐酸中,搅拌让他们充分反应后,过滤。取滤液加入少量铁粉,无任何现象。则下列判断正确的是 ( )
A.滤渣中不含铜 B.滤渣可能是铜和铁的混合物
C.滤液中含FeCl2和CuCl2 D.滤液中含FeCl2和HCl
20.图l3-9表示四种操作过程,其中表示正确的图像是 ( )

A.向pH=1的酸溶液中不断加水
B.向pH=1的硫酸溶液中逐滴加入pH=13的氢氧化钠溶液
C.某温度下,向一定量的水中持续加入食盐并不断搅拌(m表示加入食盐的质量,A%表示溶质质量分数)
D.等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量M与反应时问t的关系图
三、填空题(本题包括7小题,每空1分,共27分)
21.我们在初中化学里学过的一些物质,在实际生活中有重要的用途。现有以下4种物质:硝酸钾、稀硫酸、硫酸铜、干冰,请用它们(或其主要成分)的化学式填空。
(1)可用于配制杀菌剂波尔多液:
(2)可用于除去铁锈:
(3)可用于人工降雨:
(4)可作为复合肥使用:
22.某化学反应可用漫画图l3-10表示,请根据图示回答:

(1)该反应的基本反应类型属于 反应。
(2)该反应生成的物质属于 (填物质分类)。
(3)分析以上漫画图示,你还能总结出的一条结论是
23.把A、B、C、D四种纯净物放在一密闭容器中,在一定条件下充分反应,反应前后各物质的质量见下表:
物 质
A
B
C
D
反应前质量/9
2
24.5
2
1
反应后质量/9
16.9
O
2
未知
回答下列问题:
(1)反应后D的质量是 g;
(2)C物质可能是 (填写反应物、生成物或催化剂);
24.图l3-11是一种打火机的示意图。请根据有关信息回答下列问题:

(1)构成打火机的材料中属于合成材料的是
a.合金 b.塑料
(2)其燃料的主要成分丁烷(C4H10)属于 (填“有机”或“无机”)化合物。丁烷在通常状况下呈气态,请用分子的基本性质解释丁烷气体能被压缩成液体的原因: _。
(3)打火机挡风罩通风孔的作用是使空气流通,说明燃料燃烧必须与 接触。若通风孔通气不良,可能造成打火机无法起火或燃料不完全燃烧而生成有毒气体,既浪费了燃料又污染了环境。用打火机点火是利用燃料燃烧将化学能转化为 能。
25.现有甲、乙、丙、丁四种化合物。已知这四种化合物都是Na、S、C、H、O五种元素中的 种组成。并且甲+乙=丙+ H2O,乙+丁―,丙+ H2O + CO2,其余两两混合均不反应。根据上述提供的物质变化和物质组成的信息,试写出它们的化学式: 甲 乙 丁 。
26.(1)古代铜币表面绿色铜锈的主要成分是Cu2 (OH)2CO3,文物鉴定人员常用酸验法鉴别铜锈真伪;用细玻璃棒蘸取少许稀盐酸,涂擦在需要鉴别可疑铜锈的部位,若有气泡产生则初定为铜锈,反应的化学方程式为 。
(2)某厂采用联合法生产硫酸铜、硫酸亚铁作饲料添加剂,主要步骤如图l3-l2所示:
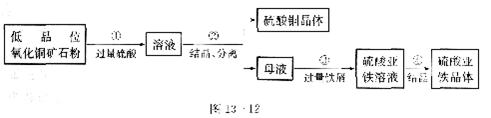
写出图中①、③反应的化学方程式:
①
③ 。
27.地球上的淡水资源是十分有限的。人类生产、生活造成的水体污染加剧了水资源危机。常州市的水资源十分丰富,但作为常州明珠的涌湖、长荡湖已受到不同程度污染。
(1)水体富营养化是常州市水环境的主要问题之一。水体富营养化是指水体中含氮、磷的化合物过多,这些化合物是水生植物生长、发育的养料。
①蛋白质是主要的含氮污染物,蛋白质在水中分解:蛋白质一氨基酸一氨(NH3),氨在微生物作用下,与溶解在水中的氧气反应,生成亚硝酸(HNO2)和水,反应的化学方程式为 ,弧硝酸进一步在微生物作用下与氧气反应生成硝酸,并以硝酸盐的形式作为水生植物的养料。
②含磷化合物主要来源于洗涤剂和不合理使用磷肥。洗涤剂中有一种成分的化学式为Na5PxOy,若P的化合价为+a,则a和x,y的关系是:a= 。
③白天受阳光照射,充足的养料使绿藻等水生植物迅速繁殖,水体变绿,光合作用的化学方程式是 。晚间由于污染物耗氧和水生植物的 作用,使水中的含氧量急剧下降,会 造成鱼类等水生动物因缺氧而死亡。另外,大量水生植物的残骸腐烂分解出有毒物质,使水质更加恶化。
(2)含酸、碱、重金属离子的工业废水也是重要的水体污染物。如果要处理某工厂产生的酸性污水,你建议用NaOH还是Ca(OH)2进行处理?,理由是:
四、实验题(本题包括3小题,每空1分,共25分)
28.某实验小组只用酚酞试液就可以鉴别稀盐酸、碳酸钠溶液和水三种试剂。他们填写的部分实验报告如下,请你帮助填写完整。
实验步骤
实验现象
实验结论
①取少量三种试剂于三支试管中,分别滴加2~3滴酚酞试液
一支试管中酚酞试液变红
色,另两支试管中无明显现象
②
29.小兵同学在化学实验室发现一瓶盛有无色溶液的试剂瓶,其标签严重破损。诉他,这瓶试剂可能是硫酸、硫酸钠、硫酸镁溶液中的一种。小兵同学通过查阅资料得知,常温下这三种物质的溶解度见下表:

物质
H2SO4
Na2SO4
Mg SO4
溶解度/g
与水任意比互溶
19.0
39.0
小兵同学根据上述信息分析认为此溶液一定不是 溶液。为确定其成分,该同学对此溶液进行如下实验探究:
[提出假设]该溶液可能是 。
[实验验证]
实验步骤
实验现象
实验结论
30.课外化学兴趣小组的同学利用某化工厂的废碱液(主要成分为Na2CO3,还含有少量NaCl,其他杂质不计)和石灰乳为原料制备烧碱,并对所得的烧碱粗产品的成分进行分析和测定。
[粗产品制备]
(1)将废碱液加热蒸发浓缩,形成较浓的溶液,冷却后与石灰乳混合,发生反应的化学方程式为 。
(2)将反应后的混合物过滤,得到的滤液进行蒸发结晶,制得NaOH粗产品。
[粗产品成分分析]
(1)取适量粗产品溶于水,滴加Ba(NO3)2溶液出现白色浑浊,发生反应的化学方程式为 ,该粗产品中一定不含有 ,理由是
(2)该小组同学通过对粗产品成分的实验分析,确定该粗产品中含有三种物质。
[粗产品含量测定]
Na2CO3含量的测定:
(1)该兴趣小组的同学设计了图l3-14所示的实验装置。取10.

[说明]碱石灰是CaO与NaOH的固体混合物。E装置中的饱和NaHCO3溶液是为了除去二氧化碳气体中的氯化氢,发生的反应为
NaHCO3+HCl==NaCl+ H2O +CO2
(2)操作步骤
①连接好装置,检查气密性;②打开弹簧夹C,在A处缓缓通入一段时间空气;③称量G的质量;④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;⑤打开弹簧夹C,再次缓缓通人一段时间空气;⑥再次称量G的质量,得前后两次质量差为0.
(3)问题探究
F中的试剂应为 ,B装置的作用是
,H装置的作用是 。若没有H装置,则测定的Na2CO3的质量分数会 (填“偏大”、“偏小”或“不变”)。事实上
(4)数据计算
根据正确值0.
该小组同学又另取
五、计算题(本题8分)
31.现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图l3-15所示。请根据有关信息计算:
(1)该试剂瓶中硫酸溶液的质量是 g。工人小李用该浓硫酸配制20%的稀硫酸,以清洗钢铁表面的铁锈。他在配制该溶液时所用98%的浓硫酸与水的质量比应该为 。
(2)某固体物质由氯化钠和氯化钡组成,取32.
(3)若加入的稀硫酸刚好使沉淀达最大量时,将


所得混合物过滤、洗涤,得滤液2009(过程中损耗忽略不计),计算该滤液中溶质的质量分数。(若溶液中含有多种溶质,则每种溶质的质量分数为该溶质的质量与溶液总质量之比)