2008年聊城市阳谷县第一实验中学九年级
化学试卷
(时间:40分钟,满分:40分)
相对原子质量:H:1 C:12 O:16 Cl:35.5 Ba:137 Ag:108
第Ⅰ卷(选择题,共16分)
一、选择题(本大题包括10小题,其中第l―4小题每小题1分,第5―10小题每小题2分,共16分,每小题只有一个选项符合题意)
1.下列造成空气污染的因素主要是由于物理变化引起的是( )
A.节日燃放烟花爆竹产生烟尘
B.建筑施工导致尘土飞扬
C.生活垃圾的焚烧产生的有害气体
D.生物的腐烂放出一氧化碳
2.下列化学物质与人的生命活动有关的叙述中,不正确的是( )
A.糖类是人类食物中主要的供能物质
B.夏天出汗多,要及时补充食盐和水,以调节体液平衡
C.一氧化碳会与血液中的血红蛋白结合,使人中毒
D.人体缺乏钙、铁、碘元素会引起许多疾病,所以饮食中摄入得越多越好
3.烧杯是常用的实验仪器。下列实验中需要使用烧杯的是( )
①稀释浓硫酸
②量取15ml液体
③过滤
④用固体药品配制一定溶质质量分数的溶液
A.①②③ B.②③④
C.①③④ D.①②④
4.在学习化学的过程中,有些同学经常对所学知识进行归纳,如化石燃烧主要包括煤、石油、天然气。下列知识的归纳有错误的一组是( )
化石燃料
煤、石油、天然气……
A
干燥剂
石灰石、浓硫酸、生石灰……
B
合金
不锈钢、焊锡、生铁
C
营养素
蛋白质、无机盐、维生素
D
氧化物
干冰、水、氧化镁
5.足球是一项运动量大且易受伤的球类运动。在运动过程中当运动员肌肉受伤时,队医随即对准球员的受伤部位喷射药剂氯乙烷(化学式为C2H5Cl,沸点为l
A.氯乙烷是由碳、氢、氯三种元素组成的
B.乙烷是由2个碳原子、5个氢原子和1个氯原子构成的
C.氯乙烷中碳、氢、氯三种元素的质量比为48∶10∶71
D.氯乙烷用于冷冻麻醉与其沸点较低、易挥发吸热有关
6.将N2、CO、HCl气体的混合物依次通过NaOH溶液、浓硫酸、灼热的氧化铜。假定每次处理均能完全反应(或吸收),则最后排出的气体为( )
A.HCl、CO2 B.N2、CO
7.将下列各组内的物质混合,充分反应后过滤,所得溶液的质量比反应前溶液质量减少的是( )
A.Zn和稀盐酸 B.Cu和AgNO3溶液
C.Cu(OH)2和稀硫酸 D.Na2CO3固体和稀盐酸
8.除去下列物质中所含杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是( )
选项
待提纯的物质
选用的试剂
操作方法
A
MnO2(HCl)
水
溶解、过滤、结晶
B
CO2(CO)
氧气
点燃
C
Cu(CuO)
稀盐酸
溶解、过滤、洗涤、干燥
D
CuSO4(H2SO4)
氢氧化钠溶液
过滤
9.在“绿色化学”工艺中,理想状态是反应物中的原子全部转化为欲得到的产物,即原子的利用率为100%,从根本上减少乃至杜绝污染。下列做法符合“绿色化学”的是( )
A.农民就地焚烧秸秆 B.深埋含镉、汞的废电池
C.工业制酒精C2H4+H2O C2H6O D.化工生产中的废气向高空排放
C2H6O D.化工生产中的废气向高空排放
10.下列图像不能正确反映其对应操作的是( )
A
B
C
D
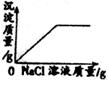
在一定量AgNO3溶液中逐滴加入NaCl溶液
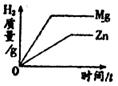
等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应
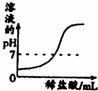
向NaOH溶液中逐滴加入稀盐酸
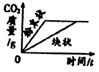
等质量的CaCO3分别与等体积等质量分数的稀盐酸(足量)反应
第Ⅱ卷(非选择题,24分)
二、填空与简答题(本题包括3小题,共8分)
11.(3分)化学就在我们身边,它能改善我们的生活。请从“A.干冰;B.氢气;C.尿 素;D.明矾;E.蛋白质;F.硝酸钾;G.石油;H.纯碱;I.烧碱”中选择适当的物质填空(填字母)。
(1)常用于净水的物质是 ;
(2)被誉为“工业的血液”的是 ;
(3)构成人体细胞的基础物质是 ;
(4)农业上可用作复合肥的是 ;
(5)被称为理想“绿色能源”的是 ;
(6)侯氏联合制碱法中的“碱”是 。
12.(3分)下面是实验室里常用的仪器,根据题中要求填空。
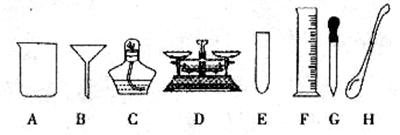
(1)写出指定仪器的名称:
C ,E 。
(2)在粗盐提纯实验中,进行 时(填操作名称)用到仪器B进行蒸发时除了用到铁架台、铁圈、玻璃棒和上述提供的仪器外,还缺少的仪器的是 。
(3)配制
13.(2分)图1是甲、乙两种物质的溶解度曲线,图2所示两个烧杯中各盛有
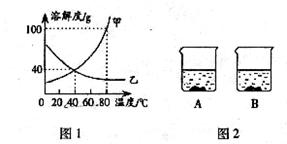
请你通过分析,回答下列问题:
(1)溶解度随温度升高而增大的物质是 (填“甲”或“乙”)。
(2)
(3)
(4)当温度由
三、实验探究题(本题包括2个小题,共11分)
14.(5分)有一包粉末,可能由KCl、K2SO4、K2CO3、CuCl2、MgCl2中的一种或几种物质组成。现做如下实验:
实验①:取少量粉末,加水溶解后得到无色透明溶液。
实验②:取①所得溶液少许,加入氢氧化钠溶液后看不到明显现象。
实验③:取①所得溶液少许,加入适量硝酸钡溶液后出现白色沉淀,过滤后,在沉淀中加入适量稀硝酸,沉淀全部溶解。
根据以上实验,请回答:
(1)原粉末中一定没有 ,一定有 。
(2)原粉末中可能有 ,为了验证可能含有的成分是否存在。请你设计实验证明:
操作
现象
结论
含有该物质
15.(6分)物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象。某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH值逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
(1)用pH试纸测定溶液的pH时,正确的操作是: 。
(2)简述强调“测得的pH小于
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,可观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了。该小组对这种意外现象的原因作了如下猜想:
①可能是酚酞溶液与空气中氧气反应,使红色消失;
②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失。
(1)为验证猜想①,该组同学做了如下实验:将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液。实验中“加热”和“滴入植物油”目的是 。实验结果证明酚酞溶液红色消失与空气中的氧气无关。
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色,由此可得出以下两点结论:
结论1:说明Na2CO3溶液呈 性;
结论2:说明酚酞溶液红色消失与空气中的二氧化碳无关。
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度很大时,就会出现上述意外现象。请设计实验证明该方案中取用的NaOH溶液浓度过大:
①实验方法 ,
②观察到的现象 。
四、计算题(共5分)
16.现有一含杂质的固体氯化钡(BaCl2)样品(杂质不溶于水),取
(1)生成白色沉淀多少克?
(2)
(3)样品中氯化钡的质量分数。