2007年枣庄市中等学校招生考试理科综合化学试题
本试题分第Ⅰ卷和第Ⅱ卷两部分。第Ⅰ卷1―4页为选择题.50分;第Ⅱ卷5―12页为非选择题.100分。全卷共12页。满分l50分。考试时间为120分钟。
第I卷(选择题共50分)
注意事项:
1.答第I卷前.务必将自己的姓名、准考证号、考试科目和试卷类型涂写在答题卡上?并在本页正上方空白处写上姓名和准考证号。考试结束,将试题和答题卡一并交回。
2.答第I卷时。每题选出答案后.用2B铅笔把答题卡上对应题目的答案标号(ABCD)涂黑.如需改动.先用橡皮擦干净.再改涂其他答案标号。不能答在试卷上。
可能用到的相对原子质量:
H l C 12 N14 O16 S 32 Cl 35.5 Cu 64 Ca 40
本卷共25个小题.每题2分。共50分。在下列每小题给出的四个选项中。只有一项是符合题目要求的。
13.以下是一些常用的危险品标志,装运乙醇的包装箱应贴的标志是

14.现有5种物质:①浓盐酸 ②烧碱 ③食盐 ④浓硫酸 ⑤铁 把它们长期露置在空气中,其中发生化学变化且质量增加的是
A.①② B.②⑤ C.③④ D.③⑤
15.今年5月,我市某区发生了一起液化气罐爆炸事故,它再次给广大液化气用户敲响了警 钟。液化气的主要成分在空气中充分燃烧的化学方程式为:X+5O2 3CO2+4H2O 下列对X的判断不正确的是
3CO2+4H2O 下列对X的判断不正确的是
A.X是一种有机化合物 B.X一定含碳、氢、氧三种元素
C.X是一种重要的燃料 D.X的化学式是C3H8
16.我国商代已制造出精美的青铜器,春秋战国时期已会冶铁和炼钢。人类开发利用金属单 质的时间顺序与金属活动性的强弱有着某种内在联系。由此推断,下列金属中,人类开发利用最晚的是
A.Al B.Fe C.Zn D.Cu
17.正确的化学实验操作对实验结果、人身安全非常重要。下图中的实验操作正确的是

18.20世纪20年代,就有人预言可能存在由4个氧原子组成的氧分子(O4),但一直没有得到证实。最近,意大利一所大学的科学家使用普通氧分子和带正电的氧离子制造出了这种 新型氧分子,并用质谱仪探测到了它的存在。下列叙述中正确的是
A.O4是一种新型的化合物 B.一个O4分子中含有2个O2分子
C.O4和O2的性质完全相同 D.O4和O2混合后形成的是混合物
19.图表资料可以为我们提供很多信息,下列从图表中获取的信息及应用不正确的是
A.根据金属活动性顺序表,判断金属是否容易被盐酸腐蚀
B.根据金属的熔点数据表。判断金属的导电性强弱
C.根据溶解度曲线图。选择从溶液中获得晶体的方法
D.根据元素周期表,查找元素的原子序数、元素符号、相对原子质量等信息
20.食品安全与人体健康密切相关。下列做法中对人体健康有危害的是
A.蒸馒头时加入适量的纯碱
B.在装小食品的袋子中充入氮气
C.用石灰水保存鲜蛋
D.制香肠时加过量的亚硝酸钠
第Ⅱ卷(非选择题共100分)
注意事项:
1.用钢笔或圆珠笔直接将答案写在试卷上。
2.答卷前将密封线内的项目填写清楚.并在试卷第10页的右下角准确填写座号。
二、化学题:本大题包括3个题,共34分.
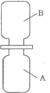
38.(8分)化学课上老师表演了一个小魔术“无中生有”:相同条件下,向A、 B两个体积相同的集气瓶中分别充满无色的硫化氢(H2S)气体和二氧化硫气体。如图所示,抽开毛玻璃片,瓶口对紧,颠倒几次,使两种气体充分混合。一会儿,观察到两瓶内壁附着淡黄色固体颗粒。请回答下列问题:
(1)若用“●”表示氢愿子、“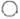 ”表示氧原子、“
”表示氧原子、“ ”表示硫原子,上述反应过程可用下图表示
”表示硫原子,上述反应过程可用下图表示

该反应的化学方程式为______________________________________________;
其中硫化氢、二氧化硫中硫元素的化合价分别为______________________________.
(2)如果这两个瓶子是质地较软的塑料瓶,我们将会观察到塑料瓶变瘪了,原因是_________
(3)已知:相同条件下.相等体积的气体所含的分子数目相等。反应完毕,瓶中剩余的气体为______,处理该气体的方法是______。
39.(5分)只用钠、氧、硫、氢四种元素中的一种或几种组成符合要求的五种物质,并各写出一个化学式填入下图中的虚线椭圆内。
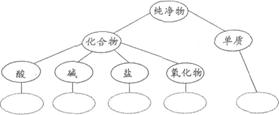
40.(6分)
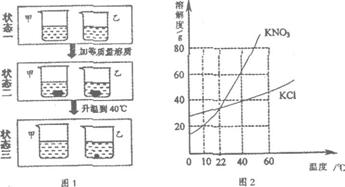
(1)当温度(t)的取值范围为______时,硝酸钾的溶解度大于氯化钾的溶解度。
(2)烧杯甲盛放的是______溶液。
(3)状态三时,两个烧杯中溶剂水的质量较小的是______。(填“甲”或“乙”)
(二)实验题(本题包括2小题。共l0分)
41.(4分)把一小包铁粉放入一定量的硝酸铜溶液中,使其充分反应后,过滤、洗涤、干燥,得到固体。请你对固体的成分进行探究。
(1)猜想:固体的成分可能是______
(2)实验:请设计实验验证你的猜想。说明实验过程、现象和结论
42.(6分)为了制备少量的氧气,某实验小组分三个阶段开展了一系列的工作:
第一阶段:查阅文献资料,获得了下列信息:双氧水、氯酸钾、高锰酸钾等含有氧元素的物质在一定条件下分解都可以产生氧气。其中双氧水溶液价格最低。在常温下就能够分解放出氧气,该过程无副产物;氯酸钾价格较高,分解较困难,且常伴有副产物;高锰酸钾价格较高,加热即可快速分解。二氧化锰能加速上述三种物质的分解。
根据上述信息,实验小组选择双氧水溶液和二氧化锰混合制备氧气。
第二阶段:到实验室准备实验用品,安装实验仪器,进行制备实验。可供选择的实验装置如下:
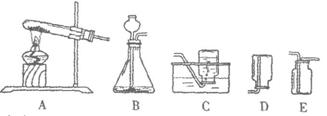
第三阶段:实验完毕,洗刷实验仪器,整理实验用品。问题:
(1)要制取一瓶氧气,应选择的实验装置是______ (填写字母代号);组装好实验装置后应首先进行__________________。
(2)有气体产生的化学反应在有限的空间里发生时,如果反应过快,容易引起爆炸。你认为该实验中可以采取哪些措施预防爆炸?(列举两条)
(3)回顾整个工作过程,你认为在准备工作阶段除应考虑药品的价格、制氧反应的难易、制氧过程的安全性等问题外,还应考虑哪些问题?(列举两条)
(三)计算题(本题包括l小题.共5分)
43.(5分)某样品为铜和氧化铜的混合物,为测定其中氧化铜的质量分数,取
序号
加入稀盐酸的质量/g
剩余固体的质/g
第1次
20
16
第2次
20
12
第3次
20
8.5
第4次
20
n
(1)上表中n的数值为______。
(2)样品中氧化铜的质量分数是______。
(3)求盐酸中溶质的质量分数。