2008年秋季湖北省黄冈中学高一化学期末考试试题
本试卷分第Ⅰ卷和第Ⅱ卷共108分,考试时间90分钟
可能用到的相对原子质量是:H:1 C:12 O:16 Na:23 Cl:35.5 K:39
Ca:40 Mn:55 Fe:56 Br:80
第Ⅰ卷(选择题,共49分)
一、选择题(本题包括5小题,每小题2分,每小题只有一个选项符合题意)
1.著名化学家、诺贝尔化学奖获得者Glenn Theodore Seabory1979年在美国化学会成立100周年大会上指出:“化学,是人类进步的关键!”。学习和研究化学是为了更好的认识世界。下列涉及的内容一般不属于化学研究范围的是
A.研究一种新材料的性质和用途 B.研究一种新微粒的组成和结构
C.研究一种新药品的合成 D.研究一种新物质的运动规律
2.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,
B.氧气和臭氧的混合物
C.
D.
3.关于Na+和Na的性质叙述正确的是
A.都具有金属光泽 B.都是强还原剂
C.焰色反应现象相同 D.电子层结构相同
4.实验室制取下列各组气体,所用气体发生装置相同的是
A.氢气和二氧化碳 B.氢气和氧气
C.氯气和氧气 D.氯气和氢气
5.下列物质用途不正确的是
A.溴化银可用于制胶片和有色玻璃 B.过氧化钠可用于漂白织物、羽毛等
C.碘化银可用于人工降雨 D.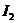 可以用于配制含碘食盐
可以用于配制含碘食盐
二、选择题(本题包括8小题,每题3分,共24分.每小题有一至两个选项符合题意.只有一个正确选项的,多选不给分.有两个正确选项的,选对一个给1分,选错一个不给分)
6.在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象
和结论一致且正确的是
A.加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在
B.溶液呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在
C.加入盐酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在
D.加入NaOH溶液,氯水浅黄绿色消失,说明有HClO分子存在
7.下列各组溶液中,不用任何其它试剂即可鉴别的是
A.HF、HCl、HBr、HI B.KMnO4、CuCl2、FeCl3,NaCl
C.KNO3、KI、AgNO3、Na2CO3 D.溴水、NaCl、NaBr、KI
8.下列离子方程式的书写中正确的是
A.等体积、等浓度的KHSO4溶液与Ba(OH)2溶液反应:
Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B.在次氯酸中加入碳酸钠:2HClO+CO32-=2ClO-+H2O+CO2↑
C.钾与水反应:2K+2H2O=2K++2OH-+H2↑
D.氯化钠溶液中通入氟气:F2+2Cl-=
9.一辆载有约35吨液氯的槽罐车与一辆货车相撞,导致槽罐车中液氯大面积泄漏,造成多人伤亡。下列处理方法和过程合理的是
A.将人群转移到地势较低的地方,等待营救
B.将槽罐车推入附近的水塘中,撒上石灰
C.用高压水枪向空中喷洒大量浓氨水溶液
D.被转移人群可戴上用NaOH处理过的口罩
10.比较是化学学习中的一种重要方法。下列各组比较中不正确的是
A.在相同条件下的溶解度:NaHCO3>Na2CO3
B.热稳定性:HF>HCl>HBr>HI
C.氧化性:F2> Cl2 > Br2 >I2
D.碳酸钠溶液与稀盐酸互滴时,两种操作现象相同
11.为除去括号内的杂质,所选用的试剂或方法不正确的是
A.Na2CO3粉末(NaHCO3),加热直至固体质量不再减少
B.NaHCO3溶液(Na2CO3),向溶液中通入过量的CO2气体
C.CO2 (HCl),将气体依次通过Na2CO3溶液和浓硫酸中
D.H2 (HCl),将气体通入碱石灰中
12.下列相关卤素的叙述正确的是
A.卤素离子(X-)只有还原性而无氧化性
B.某元素由化合态变成游离态,该元素一定被氧化
C.失电子难的原子获得电子的能力一定强
D.卤素最高价氧化物的分子式都为X2O7
13.取碘水四份于试管中,编号为Ⅰ、Ⅱ、Ⅲ、Ⅳ分别加入汽油、CCl4、酒精、NaCl溶液,振荡后静置,现象正确的是
A.Ⅰ中溶液分层,下层呈紫红色
B.Ⅱ中溶液分层,下层呈紫红色
C.Ⅲ中溶液分层,下层呈棕黄色
D.Ⅳ中溶液不分层,溶液由棕黄色变成黄绿色
三、选择题(本题包括5小题,每小题3分,共15分,只有一个选项符合题意)
14.甲、乙、丙三种液各含有一种X-(Cl-、Br-、I-)。 向甲中加淀粉溶液和氯水,则溶液变为橙色,再加丙溶液,颜色无明显变化。则甲、乙、丙依次含有
A.Br-、Cl-、I- B.Br-、I-、Cl-
C.I-、Br-、Cl- D.Cl-、I- 、Br-
15.据报导,在全国各地发生过多次因混合洁污剂引起氯气中毒的事件。据此推测相混合的洁污剂中最有可能含
A.ClO4-、Cl-、Na+ B.ClO-、Cl-、H+ C.NaClO、NaClO3 D.NaClO、NaCl
16.用
A.1∶3 B.2∶
17.某溶液中Cl-、Br-、I-三者物质的量之比为2┱3┱4,要使溶液中Cl-、Br-、I-物质的量之比为1┱1┱1,则通入Cl2的物质的量是原溶液中I-物质的量的
A.1/2 B.1/
18.在一密封容器中盛有0.8mol Na2O2与1mol NaHCO3,将其加热到
A.0.5mol Na2CO3和1mol NaOH B.1mol Na2CO3和0.6mol NaOH
C.0.8mol Na2CO3和1mol NaOH D.只有1mol Na2CO3
第Ⅱ卷(非选择题,共59分)
四、实验题(本题包括2小题,共17分)
19.(9分)某NaCl样品中混有NaBr杂质,为了测定该NaCl样品的纯度,设计的实验过
程如下图所示:
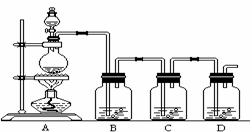 (1)下图装置是用来完成向溶液甲中通入过量Cl2的实验,在下面表格内填写装置中所放的化学药品。
(1)下图装置是用来完成向溶液甲中通入过量Cl2的实验,在下面表格内填写装置中所放的化学药品。
A
→
B
→
C
→
D
溶液甲
(2)萃取所需要的主要玻璃仪器是_______________;
(3)溶液甲中通入Cl2的化学方程式为 ;
(4)原固体样品中氯化钠的质量分数为__________________。
20.(8分)利用Na2O2与水反应能放出氧气的性质,可通过选择装置A或B来测定已部分变质的Na2O2样品中Na2O2的质量分数。
| |||||||||||||||||||||||
 D+C+O2↑:
。
D+C+O2↑:
。 5
5 13
13 5
5 13
13
 22.(8分)(1)B:Na2O2 E:NaHCO3;
22.(8分)(1)B:Na2O2 E:NaHCO3; 2Na2CO3+2NaOH+O2↑。
2Na2CO3+2NaOH+O2↑。 MnCl2+Cl2↑+2H2O;②;C
MnCl2+Cl2↑+2H2O;②;C