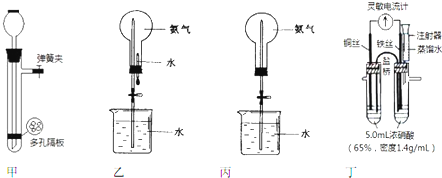
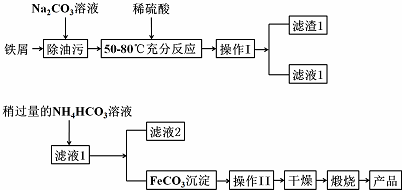
12.已知:2H2(g)+O2(g)=2H2O(l)△H=-570.0kJ/mol;
CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-280.0kJ/mol.
某H2和CO的混合气体完全燃烧放出141kJ热量,同时消耗标准状况下5.6L O2,则原混合气体中H2和CO的物质的量之比为( )
CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-280.0kJ/mol.
某H2和CO的混合气体完全燃烧放出141kJ热量,同时消耗标准状况下5.6L O2,则原混合气体中H2和CO的物质的量之比为( )
| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 2:3 |
11.下列有关说法正确的是( )
| A. | 反应2NO2═N2O4在室温下可自发进行,则该反应的△H<0 | |
| B. | 工业上电解熔融态氯化铝冶炼单质铝 | |
| C. | CH3COOH 溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$的值增大 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH 减小 |
10.下列实验误差分析错误的是( )
| A. | 用湿润的pH试纸测稀溶液的pH,测定值可能偏大 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| C. | 滴定前滴定管尖嘴部分无气泡,终点读数时有气泡,所测体积偏小 | |
| D. | 测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小 |
9.下列事实,不能用平衡移动原理解释的是( )
| A. | 硫酸工业中,增大O2的浓度有利于提高SO2的转化率 | |
| B. | 将FeS固体投入到含有Cu2+的废水中以除去Cu2+ | |
| C. | 选择合适的催化剂可提高工业合成氨的生产效率 | |
| D. | 滴有酚酞的CH3COONa溶液,加热后颜色变深 |
8.下列化学反应中反应物总能量高于生成物物总能量的是( )
| A. | CO2与炭化合 | B. | 碳酸钙分解反应 | C. | 铝热反应 | D. | 制水煤气反应 |
5.已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
| A. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{7}$amol | |
| B. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-})}$=$\frac{1}{2}$ | |
| C. | 参加反应的氯气的物质的量等于$\frac{1}{2}$amol | |
| D. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$amol≤ne≤amol |
3.化学实验操作准确性非常重要,如图分别表示四种操作,其中有两处错误的是( )
0 168754 168762 168768 168772 168778 168780 168784 168790 168792 168798 168804 168808 168810 168814 168820 168822 168828 168832 168834 168838 168840 168844 168846 168848 168849 168850 168852 168853 168854 168856 168858 168862 168864 168868 168870 168874 168880 168882 168888 168892 168894 168898 168904 168910 168912 168918 168922 168924 168930 168934 168940 168948 203614
| A. | 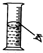 读数 | B. | 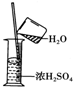 稀释 | C. |  称量 | D. |  溶解 |