10.某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度.有关的叙述正确的是( )
| A. | H2Y的电离方程式为:H2Y+H2O?H3O++HY- | |
| B. | 在该酸式盐溶液中c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) | |
| C. | HY-的水解方程式为HY-+H2O?H3O++Y2- | |
| D. | 在该酸式盐溶液中c(Na+)>c(HY-)>c(OH-)>c(H+) |
9.将相同物质的量浓度的某弱酸HX溶液与NaX溶液等体积混合,测得混合后溶液中c(Na+)>c(X-),则下列关系正确的是( )
| A. | c(OH-)<c(H+) | B. | c(HX)<c(X-) | ||
| C. | c(X-)+c(HX)=2c(Na+) | D. | c(HX)+c(H+)=c(Na+)+c(OH-) |
6.已知HF比CH3COOH易电离.关于物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液,下列说法正确的是( )
| A. | CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | |
| B. | 在相同条件下,两溶液的pH大小为:CH3COONa<NaF | |
| C. | NaF溶液中:c(H+)+c(HF)=c(OH-) | |
| D. | 两溶液相比较,CH3COONa溶液中的离子总数较多 |
5.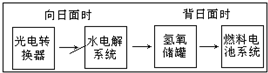 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )
 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )| A. | 燃料电池系统产生的能量实际上来自于水 | |
| B. | 该能量转化系统中的水也是可能循环的 | |
| C. | 水电解系统中的阳极反应:4OH--4e-=2H2O+O2↑ | |
| D. | 燃料电池放电时的负极反应:H2-2e-+2OH-=2H2O |
4.下列为某同学根据中学化学教材中的数据所做的判断,其中错误的是( )
| A. | 根据Ksp数据,判断长时间煮沸Mg(HCO3)2溶液所得沉淀是MgCO3还是Mg(OH)2 | |
| B. | 根据反应热数据,判断不同反应的反应速度的大小 | |
| C. | 根据Kc数据,判断某可逆反应在某一温度下是否达到平衡 | |
| D. | 根据Ka数据,判断弱酸的酸性强弱 |
3.分别向含有下列离子的溶液中加入NaOH固体(溶液体积不变),能引起离子浓度减少的是( )
| A. | Cl- | B. | OH- | C. | [Al(OH)4]- | D. | HCO3- |
2.一定条件下的密闭容器中,进行如下反应NO(g)+CO(g)?$\frac{1}{2}$ N2(g)+CO2(g),△H<0,达到平衡后,为提高该反应的反应速率和NO的转化率,采取的措施正确的是( )
| A. | 加催化剂同时升高温度 | B. | 加催化剂同时增大压强 | ||
| C. | 升高温度同时充入N2 | D. | 降低温度同时增大压强 |
1.下列叙述正确的是( )
0 168460 168468 168474 168478 168484 168486 168490 168496 168498 168504 168510 168514 168516 168520 168526 168528 168534 168538 168540 168544 168546 168550 168552 168554 168555 168556 168558 168559 168560 168562 168564 168568 168570 168574 168576 168580 168586 168588 168594 168598 168600 168604 168610 168616 168618 168624 168628 168630 168636 168640 168646 168654 203614
| A. | 强弱电解质的根本区别在于电离时是否存在电离平衡 | |
| B. | 所有的离子化合物都是强电解质,所有的共价化合物都是弱电解质 | |
| C. | 弱电解质的水溶液中只有离子,没有分子 | |
| D. | 强电解质融化状态下都能导电 |
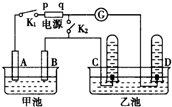 在图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重1.6g.请回答下列问题:
在图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量,电极增重1.6g.请回答下列问题: