7.用惰性电极电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是( )
| A. | 酸性AgNO3溶液 | B. | HCl溶液 | C. | 稀NaOH溶液 | D. | 酸性CuSO4溶液 |
6.下列物质属于弱电解质的是( )
| A. | CH3COOH | B. | NaOH | C. | SO2 | D. | NH4Cl |
4.下列说法正确的是( )
| A. | pH均为9的①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液,其物质的量浓度的大小顺序为①>②>③ | |
| B. | 等物质的量浓度的Na2CO3溶液和NaHCO3溶液等体积混合,所得溶液中:c(CO32-)+c(OH-)<c(H+)+c(HCO3-)+3c(H2CO3) | |
| C. | 0.1 mol•L-1KHC2O4溶液中:c(OH-)=c(H+)+c(H2C2O4)-2c(C2O42-) | |
| D. | pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(R2-)+c(HR-)=c(Na+) |
3.能正确表示下列反应离子方程式的是( )
| A. | 磁性氧化铁溶于稀硝酸:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| B. | Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| C. | 用两根铜棒电解稀盐酸:2H++2Cl-$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| D. | Na2S2O3溶液中加入稀硫酸:2S2O+4H+═SO42-+3S↓+2H2O |
2.化学与生活密切相关,下列说法正确的是( )
| A. | 使用填埋法处理未经分类的生活垃圾 | |
| B. | “地沟油”经过加工处理后可用来制肥皂 | |
| C. | 大量使用薪柴为燃料,践行低碳生活 | |
| D. | CO2、NO2或SO2的排放是形成酸雨的主要原因 |
1.为了探究化学反应中的能量变化,某同学设计了如下两个实验.
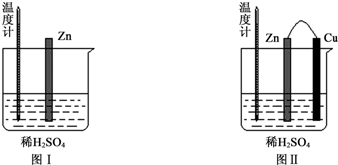
(1)图Ⅰ中发生反应的离子方程式为Zn+2H+═Zn2++H2↑,实验中温度计指示的温度逐渐升高(填“升高”或“降低”),原因是锌与稀硫酸反应是放热反应.
(2)图Ⅱ实验的实验现象如下表,请完成相应实验现象的解释.
(3)若将图中的Cu片替换为Al片,则Al片上的电极反应式为Al-3e-═Al3.

(1)图Ⅰ中发生反应的离子方程式为Zn+2H+═Zn2++H2↑,实验中温度计指示的温度逐渐升高(填“升高”或“降低”),原因是锌与稀硫酸反应是放热反应.
(2)图Ⅱ实验的实验现象如下表,请完成相应实验现象的解释.
| 实验现象 | 解释原因 |
| Cu片上产生了大量气泡 | Zn、Cu构成原电池,H+在Cu片上得电子产生氢气 |
| 温度计指示的温度无明显变化 | 反应中的化学能主要转化成了电能 |
19.下列粒子(分子或离子)均含有18个电子:
请回答下列问题:
(1)A的元素符号是K,B2-的结构示意图是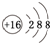 .
.
(2)C与D混合,发生反应的化学方程式为F2+2HCl═2HF+Cl2.
(3)E的电子式是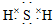 ;F的水溶液常用于消毒剂,F的化学式是H2O2.
;F的水溶液常用于消毒剂,F的化学式是H2O2.
| 粒子 | A+ | B2- | C | D | E | F |
| 组成特点 | 单核离子 | 化合物, 双核分子 | 单质, 双核分子 | 化合物, 三核分子 | 化合物, 四核分子 | |
(1)A的元素符号是K,B2-的结构示意图是
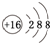 .
.(2)C与D混合,发生反应的化学方程式为F2+2HCl═2HF+Cl2.
(3)E的电子式是
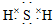 ;F的水溶液常用于消毒剂,F的化学式是H2O2.
;F的水溶液常用于消毒剂,F的化学式是H2O2.
18.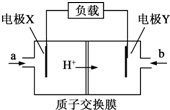 某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )
某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )
0 168440 168448 168454 168458 168464 168466 168470 168476 168478 168484 168490 168494 168496 168500 168506 168508 168514 168518 168520 168524 168526 168530 168532 168534 168535 168536 168538 168539 168540 168542 168544 168548 168550 168554 168556 168560 168566 168568 168574 168578 168580 168584 168590 168596 168598 168604 168608 168610 168616 168620 168626 168634 203614
 某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )
某氢氧燃料电池的原理如图所示.该电池的负极反应式为:H2-2e-═2H+.则下列判断中错误的是( )| A. | a处通入的是H2 | B. | 电解质溶液可能是NaOH溶液 | ||
| C. | 电极X是负极,被氧化 | D. | Y极的反应为O2+4e-+4H+═2H2O |
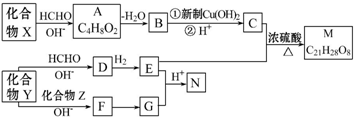
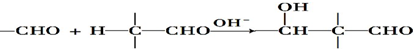
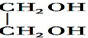 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$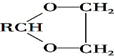 +H2O
+H2O
 .
.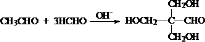 .
.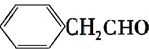
 .
.