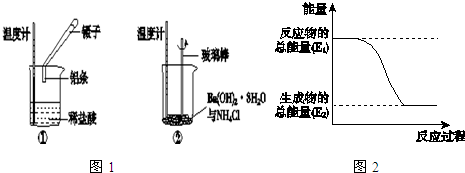
8.室温下,同种规格的铝片分别与下列物质混合,产生氢气速率最大的是( )
| A. | 0.1 mol/L的盐酸15mL | B. | 0.15 mol/L 的硫酸溶液8mL | ||
| C. | 0.2 mol/L 的盐酸12mL | D. | 18 mol/L的浓硫酸15mL |
7.使用氢氧燃料电池的汽车已在北京街头出现.下列有关该氢氧燃料电池的说法中,正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应是 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$ 2H2O | |
| C. | 氢氧燃料电池中反应放出的热量转变为电能 | |
| D. | 产物是无污染的水,属于环境友好电池 |
6.将体积比1:4的甲烷与氯气混合于一集气瓶中,加盖后置于光亮处,下列有关此实验的现象和结论叙述不正确的是( )
| A. | 产物中只有四氯化碳分子是正四面体结构 | |
| B. | 瓶中气体的黄绿色逐渐变浅,瓶内壁有油状液滴形成 | |
| C. | 若日光直射,可能发生爆炸 | |
| D. | 生成物只有CCl4、HCl |
5.元素X、Y、Z均为短周期元素且原子序数之和为35,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是( )
| A. | 三种元素的原子序数 Y>X>Z | |
| B. | 三种元素的原子半径 X>Y>Z | |
| C. | 同周期元素中X的金属性最强 | |
| D. | 同周期元素中Z的最高价氧化物的水化物酸性最强 |
4.能在溶液中大量共存的一组离子是( )
| A. | NH4+、Ag+、CO32-、Cl- | B. | Fe3+、H+、I-、HCO3- | ||
| C. | K+、Na+、NO3-、Cl- | D. | H+、Fe2+、SO42-、NO3- |
2.根据下列五种元素的电离能数据(单位:kJ/mol),回答下面各题.
(1)在周期表中,最可能处于同一族的是D
A.Q和R B.S和T C.T和U D.R和U
(2)它们的氯化物的化学式,最可能正确的是B
A.QCl2 B.RCl C.SCl3 D.UCl4
(3)下列元素中,化学性质和物理性质最像T元素的是A
A.硼(1s22s22p1) B.铍(1s22s2)C.锂(1s22s1)D.氦(1s2)
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
A.Q和R B.S和T C.T和U D.R和U
(2)它们的氯化物的化学式,最可能正确的是B
A.QCl2 B.RCl C.SCl3 D.UCl4
(3)下列元素中,化学性质和物理性质最像T元素的是A
A.硼(1s22s22p1) B.铍(1s22s2)C.锂(1s22s1)D.氦(1s2)
1.(1)在配合物[Fe(SCN)]2+中,提供空轨道接受孤对电子的微粒是Fe3+,画出配合物离子[Cu(NH3)4]2+中的配位键 .
.
(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式:(各写一种)正四面体分子CH4或CF4,三角锥形分子NH3或NF3,V形分子H2O.
(3)按要求填写下表中有序号的空格:
 .
.(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式:(各写一种)正四面体分子CH4或CF4,三角锥形分子NH3或NF3,V形分子H2O.
(3)按要求填写下表中有序号的空格:
| 元素符号 | 电子排布式 | 价层电子排布 | 在周期表中的位置 |
| ① | 1s22s22p6 | ② | ③ |
| Cr | ④ | ⑤ | ⑥ |
20.关于CO2说法正确的是( )
0 168144 168152 168158 168162 168168 168170 168174 168180 168182 168188 168194 168198 168200 168204 168210 168212 168218 168222 168224 168228 168230 168234 168236 168238 168239 168240 168242 168243 168244 168246 168248 168252 168254 168258 168260 168264 168270 168272 168278 168282 168284 168288 168294 168300 168302 168308 168312 168314 168320 168324 168330 168338 203614
| A. | 碳原子采取sp1杂化 | B. | CO2是正四面体型结构 | ||
| C. | 干冰是原子晶体 | D. | CO2为极性分子 |