��Ŀ����
������������������ͭ���Ǻ�ɫ��ĩ�����������ϡ�ijУ��ѧʵ��С��ͨ��ʵ��̽��ij��ɫ��ĩ��Fe2O3��Cu2O�������̽���������£�
�������ϣ�Cu2O��һ�ּ������������ϡ��������Cu��CuSO4��
���̽��ʵ�飺ȡ������ĩ��������ϡ�����У���������Һ�еμ�KSCN�Լ���
��1����ֻ��Fe2O3����ʵ��������_____________��
��2���������ĩ��ȫ�ܽ�������ڣ��μ�KSCN�Լ�ʱ��Һ�����ɫ����˹����е����ӷ�ӦΪ��_________________��
��3����ʵ�������ȷ����ɫ��ĩΪCu2O��Fe2O3�Ļ���ʵ��С�����ⶨCu2O��������������֪Cu2O�ڿ����м�������CuO��
�ⶨ���̣�
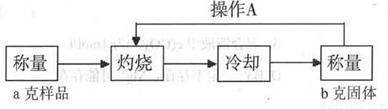
ʵ���в���A������Ϊ_____________��
���չ����У����������У��ƾ��ơ���������_____________�ȣ��г��������⣩��
��4��д���������Cu2O�����������ı���ʽ_____________��
ʵ��С�������ú�ɫ��ĩ��ȡ�ϴ����ĵ�����CuSO4?5H2O�������������ϵ�֪������Һ��ͨ��������Һ������Զ�ʹCu2+��Fe2+��Fe3+�ֱ����ɳ�����pH���£�
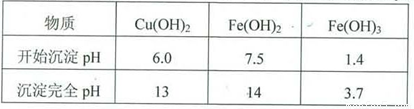
ʵ�����������Լ��ɹ�ѡ��
A����ˮ B��H2O2 C��NaOH D��Cu2(OH)2CO3
ʵ��С���������ʵ�鷽����ȡ������
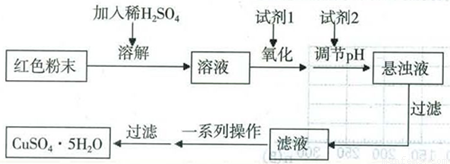
��5�����Լ���ű�ʾ���Լ�lΪ_____________���Լ�2Ϊ_____________��
��6��Ϊʲô�ȡ�����������pH����pH���Ʒ�ΧΪ���٣�
______________________________________________________________________________
������ȫ�ܽ⣬��Һ��Ѫ��ɫ��1�֣�
Fe2O3 +6H+ = 2Fe3++3H2O Cu2O+2H+ = Cu+Cu2++ H2O
2Fe3++Cu ="=" 2Fe2++Cu2+��3�֣�
���ز�����������2�֣�
 ��2�֣�
��2�֣�
�Լ�1ΪB���Լ�2ΪD����2�֣�
�����������Ӻ�ͭ���ӿ�ʼ������������ȫ��pHֵ�ܽӽ������Է��룬��������������Ϊ�����ӣ�pH���Ʒ�Χ��3.7<pH<6��������ת��Ϊ����������ȥ����2�֣�
��������
���������
��1������ɫ��ĩֻ���������������ͭ���ʳ�������������Ϊ������ȫ�ܽ⣬�������������軯����Һ�Ժ�ɫ��������Һ�ʺ�ɫ��
��2���μ����軯����Һ����죬˵����������Ӧ�꣬������������Ӧ������������ͭ����ϡ�������ɵ�ͭ���ʷ�Ӧ����Fe2O3 +6H+ = 2Fe3++3H2O Cu2O+2H+ = Cu+Cu2++ H2O
2Fe3++Cu = 2Fe2++Cu2+
��3����ʵ������У���Ҫ�ظ�ʵ����ȷ��ʵ������ȷ�ԣ�������Ҫ���ز�������ȱ�ٵ������չ����������
��4��Cu2O ��2CuO �������ء�w
144 g 16 g
m��Cu2O�� ��b-a��g
����m��Cu2O��=144g��(b-a)/16g=9(b-a)g
���Ի������Cu2O����������Ϊ9��b-a��g/ag ��100%
��5����ɫ��ĩΪFe2O3��Cu2O�Ļ����ɹ������̿�֪����������ϡ�����л���Cu���ɣ�Cu�ܽ�Fe3+��ԭΪFe2+�����õ���Һ����Fe2+�������Լ�1Ŀ����Fe2+��ΪFe3+�����������������ӣ����Լ�1Ӧѡ��B��H2O2�������Լ�2Ŀ���ǵ�����Һ��PHֵʹFe3+ת��Ϊ
Fe��OH��3������ȥ�����˵õ�����ͭ��Һ���������ƻ����������ӣ������Լ�2Ӧѡ��
Cu2��OH��2CO3��
��6�������������Ӻ�ͭ���ӿ�ʼ������������ȫ��pHֵ�ܽӽ������Է��룬��������������Ϊ�����ӣ�pH���Ʒ�Χ��3.7<pH<6��������ת��Ϊ����������ȥ��
���㣺̽�����ʵ���ɻ�������ʵĺ�����������������������ͭ����������Ҫ���������Ҫ����
���������⿼��ʵ�����Ƽ����ۣ��Լ����ʵ���ɵIJⶨ���ѶȽϴ�ע����������Ϣ���Ƕ�����֪ʶ���ۺϿ��飬��Ҫѧ��������ʵ�Ļ������ۺ����÷���������������ۺ��Խϸߣ���ҪΧ��ͭ�Ļ����������Ļ�����չ�����漰���˱�����ʣ�����ԭ���ȡ�

������������������ͭ�Ǻ�ɫ��ĩ���������ϡ�ijУһ��ѧʵ��С��ͨ��ʵ����̽��һ��ɫ��ĩ��Fc2O3��Cu2O����ߵĻ���̽���������£�
��������֪��Cu2O��һ�ּ������������ϡ��������Cu��CuSO4���ڿ����м�������CuO��
������裺����l����ɫ��ĩ��Fc2O3 ����2����ɫ��ĩ��Cu2O
����3����ɫ��ĩ��Fc2O3��Cu2O�Ļ����
���ʵ�飺ȡ������ĩ��������ϡ�����У���������Һ���ٵμ�KSCN��Һ��
��1��������1��������ʵ��������__ ��
��2�������� KSCN��Һ����Һ�����ɫ����֤��ԭ�����ĩ��һ����������������������Ϊ����˵��������____��Ͳ��������� .
��3���������ĩ��ȫ�ܽ�������ڣ��μ�KSCN��Һʱ��Һ�����ɫ����֤��ԭ�����ĩ��Fc2O3����Cu2O�Ļ�������������Ϊ____��д�����з�����������ԭ��Ӧ�����ӷ���ʽ ��̽�����죺��ʵ�������ȷ����ɫ��ĩΪFc2O3����Cu2O�Ļ���
��4��ʵ��С�����ü��ȷ��ⶨCu2O������������ȡag�����ĩ�ڿ����г�ּ��ȣ����������ٱ仯ʱ����������Ϊbg ����������Cu2O����������Ϊ
��
����������Cu2O����������Ϊ
��
��5��ʵ��С�������øú�ɫ��ĩ��ȡ�ϴ����ĵ�����CuSO4��5H2O�������������ϵ�֪����Һ��ͨ��������Һ������Զ�ʹCu2+��Fe3+��Fe2+�ֱ����ɳ�����pH���£�
|
�� �� |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
��ʼ����pH |
6.0 |
7.5 |
1.4 |
|
������ȫpH |
13 |
14 |
3.7 |
ʵ�����������Լ��ɹ�ѡ�� A����ˮ B��H2O2 C��NaOH D��Cu2��OH��2CO3
ʵ��С���������ʵ�鷽����
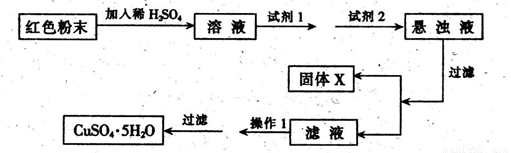
�Իش𣺢��Լ�1Ϊ___ _���Լ�2Ϊ ������ĸ����
�ڹ���X�Ļ�ѧʽΪ____���۲���IΪ_ ��
װ�����г�������ɫ���ϵ���������������������ͭ��ijѧ����ͨ��ʵ��̽��һ��ɫ��ĩ��Fe2O3��Cu2O���������̽���������£�
�������ϣ�Cu2O����ϡ��������Cu��CuSO4���ڿ����м�������CuO��
������裺
����1����ɫ��ĩ��Fe2O3��
����2����ɫ��ĩ��Cu2O��
����3��______��
���̽��ʵ�飺
ȡ������ĩ��������ϡ�����У���������Һ���ٵμ�KSCN�Լ���
��1��������1��������ʵ��������______��
��2���������ĩ��ȫ�ܽ�������ڣ��μ�KSCN�Լ�ʱ��Һ�����ɫ����֤��ԭ�����ĩ��______��
��3����һͬѧ���ü��ȷ�ȷ����ĩ����ɣ�ȡ72g�����ĩ�ڿ����г�ּ��ȣ����������ٱ仯ʱ����������Ϊ80g����ԭ�����ĩ��______��
���ۣ���ʵ�������ȷ����ɫ��ĩΪFe2O3��Cu2O�Ļ���
��4��ʵ��С�������øú�ɫ��ĩ��ȡ�����ĵ�����CuSO4?5H2O�������������ϵ�֪������Һ��ͨ��������Һ������Զ�ʹCu2+��Fe2+��Fe3+�ֱ����ɳ�����pH���£�
| ���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| ��ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |
���Լ�1Ϊ______���Լ�2Ϊ______��ѡ����ĸA��B��C��D����
�ڹ���x�Ļ�ѧʽΪ______��

 ��������ͭ�ĵ��ʡ��Ͻ��仯���������������е�Ӧ�������㷺��
��������ͭ�ĵ��ʡ��Ͻ��仯���������������е�Ӧ�������㷺��
