题目内容
在无色的强酸性溶液中能大量共存的是
| A.Mg2+、Na+、Cl-、SO42- | B.K+、 Na+、 Cl-、 Cu2+ |
| C.K+ 、Na+、NO3-、CO32- | D.Na+、Ba2+、OH-、SO42- |
A
解析试题分析:解离子共存问题注意:(1)离子之间能反应不能大量共存,反应有四类:①复分解反应:生成气体、沉淀、难电离的物质,②氧化还原反应③相互促进的水解反应④络合反应;(2)注意题目中的隐含条件:颜色、酸碱性等。A、组内离子在给定条件下不反应,能大量共存,正确;B、Cu2+在水溶液中显蓝色,错误;C、酸性条件下,H+和CO32-反应生成水和二氧化碳,不能大量共存,错误;D、、酸性条件下,H+和OH-反应生成水,Ba2+和SO42-反应生成硫酸钡沉淀,不能大量共存,错误。
考点:考查离子反应、离子共存。

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
下列化学反应所表示的离子方程式正确的是
| A.从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| B.草酸使高锰酸钾酸性溶液褪色:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O |
| C.误将洁厕灵与消毒液混合:2H++Cl-+ClO-=Cl2↑+H2O |
| D.硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42- 等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列说法一定正确的是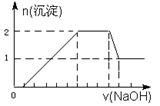
| A.一定存在H+、Mg2+、Al3+、NH+4,一定不存在Na+、SO2-4、Fe3+ |
| B.一定存在H+、Al3+、NH+4、SO2-4,可能存在Na+、Mg2+ |
| C.溶液中c(H+)∶c(Al3+):c(Mg2+)为1∶1∶1 |
| D.溶液中c(H+)∶c(SO2-4)为2∶9 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.0.1 mol·L-1的NaOH溶液:K+、Na+、SO42-、CO32- |
| B.与铝反应产生大量氢气的溶液:Na+、K+、Cl-、NO3- |
| C.0.1 mol·L-1FeCl3溶液:K+、NH4+、I-、SCN- |
| D.使紫色石蕊试液变红的溶液:Ca2+、Na+、ClO-、NO3- |
下列离子组能大量共存的是
| A.Cu2+、Na+、OH- | B.H+、Cl-、CH3COO- |
| C.Fe3+、H+、NO3- | D.K+、Ca2+、CO32- |
下列离子方程式正确的是
A.足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O 2HCO3- 2HCO3- |
B.FeSO4溶液在空气中变质:4Fe2++O2+2H2O 4Fe3++4OH- 4Fe3++4OH- |
C.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O 2Al(OH)3↓+CO32- 2Al(OH)3↓+CO32- |
D.碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+2Ca2++4OH- 2CaCO3↓+ Mg(OH)2↓+ 2H2O 2CaCO3↓+ Mg(OH)2↓+ 2H2O |
下列离子方程式书写正确的是
| A.熔融的NaHSO4电离NaHSO4=Na + + H + + SO2─ 4 |
B.HCO─ 3在水溶液中水解: HCO─ 3+H2O H3O+ + CO2─ 3 H3O+ + CO2─ 3 |
| C.AlCl3溶液中滴加过量氨水的反应: Al3+ + 4OH一= A1O─ 2+ 2H2O |
| D.电解Na2SO4溶液的阴极反应: 2 H2O + 2e一= 2OH一+ H2↑ |
下列各组离子中,能大量共存的一组是
| A.K+、NO3-、Na+、CO32- | B.Na+、Cl-、H+、HCO3- |
| C.Mg2+、Al3+、Cl-、OH- | D.Ca2+、CO32-、K+、OH- |
下列反应的离子方程式书写正确的是( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=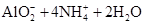 |
| B.氧化钠与水反应:O2-+H2O=2OH- |
| C.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl- |