题目内容
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象。为确定该溶液的组成,还需检验的离子是 ( )
| A.Na+ | B.SO42- | C.Ba2+ | D.NH4+ |
A
解析试题分析:本题由①知,溶液中有NH4+存在,CO32-、S2-存在于碱性溶液中,故CO32-、S2-不存在,其余离子不显酸性,由②知,溶液中没有I-,根据溶液呈电中性,一定有SO42-存在,则Ba2+不存在,故还要检验的离子是Na+。选A。
考点:考查离子检验和推断。

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
下列电离或离子方程式正确的是
A.亚硫酸的电离:H2SO3 2H++ SO3 2H++ SO3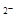 |
B.氯化铵水解的离子方程式为:NH4+ +H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.NaHCO3水解的离子方程式为:HCO3-+H2O CO3 CO3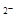 +H3O+ +H3O+ |
D.向氯化铝溶液中加入过量的氨水:A1 +3NH3·H2O= Al(OH)3↓+3NH4+ +3NH3·H2O= Al(OH)3↓+3NH4+ |
下列化学反应式书写正确的是
A.制取氢氧化铁胶体的化学方程式为FeCl3+3H2O Fe(OH)3(胶体)+3HCl Fe(OH)3(胶体)+3HCl |
B.亚硫酸在溶液中的电离方程式为H2SO 2H++SO32- 2H++SO32- |
C.NaHCO3水解的离子方程式为HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
| D.电子工业印刷电路反应式为2Fe3++Cu=Cu2++2Fe2+ |
运用有关概念判断下列叙述正确的是
| A.1molH2燃烧放出的热量为H2的燃烧热 |
| B.Na2SO3与H2O2的反应为氧化还原反应 |
C. 互为同系物 互为同系物 |
| D.BaSO4的水溶液不易导电,故BaSO4是弱电解质 |
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol·L-1 HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是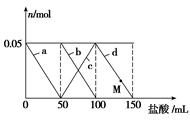
| A.a曲线表示的离子方程式为:AlO2-+H++H2O=Al(OH)3↓ |
| B.b和c曲线表示的离子反应是相同的 |
| C.M点时,溶液中沉淀的质量为3.9 g |
| D.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2 |
下列各组离子在通入SO2前后均能大量共存的是
| A.Ba2+、K+、Br-、Cl- | B.Na+、Cu2+、OH-、SiO32- |
| C.NH4+、Al3+、Br-、AlO2- | D.Li+、H+、NO3-、SO42- |
下列各组离子可能大量共存的是
| A.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br- |
| B.遇pH试纸变红色的溶液:Fe2+、S2O32-、SO42-、Na+ |
| C.水电离出的c(H+) ?c(OH-) =10-28的溶液:Na+、S2-、NO3-、SO32- |
| D.能使KSCN显红色的溶液:Na+、NH4+、AlO2-、CO32- |
下列反应的离子方程式正确的是
A.铝片跟氢氧化钠溶液反应:Al+2OH-=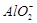 +H2↑ +H2↑ |
B.硫酸镁溶液跟氢氧化钡溶液反应: +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| C.碳酸钙跟醋酸反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ |
D.铜片跟稀硝酸反应:Cu+ +4H+=Cu2++NO↑+2H2O +4H+=Cu2++NO↑+2H2O |
下列微粒能够大量共存的是( )
| A.在pH=14的溶液中:HCO3-、Cl-、SO32-、K+ |
| B.在无色透明溶液中:Cu2+、K+、SO42-、Cl一 |
| C.在苯酚溶液中:Br-、Fe3+、NO3-、Cl- |
| D.在新制Cu(OH)2悬浊液中: CH3CHO、C2H5OH、SO42-、Na+ |