题目内容
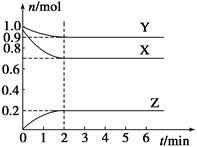
某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z。反应2min后,测得参加反应的X2为0.6mol/L,用Y2的变化表示的反应速率v(Y2)=0.1mol/(L·min),生成的c(Z)为0.4mol/L,则该反应的化学方程式是( )
A.X2+2Y2 2XY2 2XY2 | B.2X2+Y2 2X2Y 2X2Y |
C.3X2+Y2 2X3Y 2X3Y | D.X2+3Y2 2XY3 2XY3 |
C
题目要求根据一定物质的浓度变化及物质的化学反应速率来确定物质反应的化学方程式。解题时需要利用不同物质的化学反应速率与化学方程式计量数之间的关系进行逆向思维。
参加反应的X2,即为在反应中X2物质的浓度变化,则X2表示的反应速率为:v(X2)=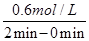 =0.3mol/(L·min);用Z表示的化学反应速率v(Z)=
=0.3mol/(L·min);用Z表示的化学反应速率v(Z)=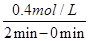 =0.2mol/(L·min),故X2,Y2和Z反应速率之比即化学方程式中物质的化学计量数之比为:v(X2)∶v(Y2)∶v(Z)=0.3mol/(L·min)∶0.1mol/(L·min)∶0.2mol/(L·min)=3∶1∶2。
=0.2mol/(L·min),故X2,Y2和Z反应速率之比即化学方程式中物质的化学计量数之比为:v(X2)∶v(Y2)∶v(Z)=0.3mol/(L·min)∶0.1mol/(L·min)∶0.2mol/(L·min)=3∶1∶2。
根据原子守恒,可确定Z的化学式为:X3Y。故可得出反应的化学方程式。
参加反应的X2,即为在反应中X2物质的浓度变化,则X2表示的反应速率为:v(X2)=
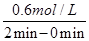 =0.3mol/(L·min);用Z表示的化学反应速率v(Z)=
=0.3mol/(L·min);用Z表示的化学反应速率v(Z)=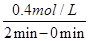 =0.2mol/(L·min),故X2,Y2和Z反应速率之比即化学方程式中物质的化学计量数之比为:v(X2)∶v(Y2)∶v(Z)=0.3mol/(L·min)∶0.1mol/(L·min)∶0.2mol/(L·min)=3∶1∶2。
=0.2mol/(L·min),故X2,Y2和Z反应速率之比即化学方程式中物质的化学计量数之比为:v(X2)∶v(Y2)∶v(Z)=0.3mol/(L·min)∶0.1mol/(L·min)∶0.2mol/(L·min)=3∶1∶2。根据原子守恒,可确定Z的化学式为:X3Y。故可得出反应的化学方程式。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
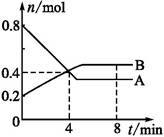
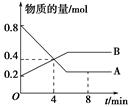
 xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1mol/(L·min)。求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1mol/(L·min)。求: I3-(aq),其平衡常数表达式为________。
I3-(aq),其平衡常数表达式为________。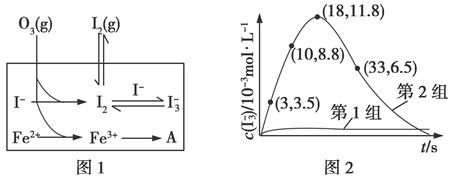
 pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a mol/L,同时C的浓度增加了2a/3 mol/L,又测得平均反应速率v(C)=2v(B)。达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为( )
pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a mol/L,同时C的浓度增加了2a/3 mol/L,又测得平均反应速率v(C)=2v(B)。达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为( )  2NH3(g)在10 L的密闭容器中进行,测得
2NH3(g)在10 L的密闭容器中进行,测得