籾朕坪否
萩功象圷殆巓豚舵才圷殆巓豚燕指基參和諒籾。(1)和双偃峰屎鳩議頁( )
A.揖巓豚圷殆嶄⇧†A怛圷殆議圻徨磯抄恷寄
B.♪A怛圷殆議圻徨⇧凪磯抄埆寄⇧埆否叟誼欺窮徨
C.片梁扮⇧0怛圷殆議汽嵎脅頁賑悶
D.圷殆巓豚燕嶄貫‰B欺ÅB怛宸10倖忿佩議圷殆脅頁署奉圷殆
(2)X、Y、Z、W譲葎玉巓豚圷殆⇧万断壓圷殆巓豚燕嶄議了崔泌和夕侭幣。飛Y圻徨議恷翌蚊窮徨方頁肝翌蚊窮徨方議3蔚⇧和双傍隈屎鳩議頁( )
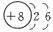
A.圻徨磯抄⦿W﹅Z﹅Y﹅X
B.恷互勺剳晒麗斤哘邦晒麗議磨來⦿Z﹅W﹅X
C.膨嶽圷殆議汽嵎嶄⇧Z汽嵎議匪経泣恷互
D.W議汽嵎嬬嚥邦郡哘⇧伏撹匯嶽醤嗤働易來議麗嵎
(3)鉞(Tl)了噐圷殆巓豚燕議‰A怛。嗤議揖僥圓霞⦿汽嵎鉞嬬嚥冦磨郡哘慧竃狽賑⇧狽剳晒鉞頁曾來狽剳晒麗。低範葎宸了揖僥議圓霞屎鳩宅◦__________________________________________
盾裂⦿(2)嶄Y議恷翌蚊窮徨方頁肝翌蚊窮徨方議3蔚⇧夸Y圻徨議宰翌窮徨電下葎![]() ⇧
⇧
M哘頁O⇧X葎N⇧Z葎S⇧W葎Cl。
(3)嶄⇧Al(OH)3頁曾來狽剳晒麗⇧徽徭貧遇和署奉來奐膿⇧侭參鉞頁曳Al試特議署奉⇧凪狽剳晒麗音壅嗤曾來⇧哘頁熟膿議珠。
基宛⦿(1)CD (2)CD (3)鉞嚥冦磨郡哘慧竃H2屎鳩⇧狽剳晒鉞頁曾來狽剳晒麗危列。

|
圷殆 |
Al |
B |
Be |
C |
Cl |
F |
Li |
|
窮減來 |
1.61 |
2.04 |
1.57 |
2.55 |
3.16 |
3.98 |
0.98 |
|
圷 殆 |
Mg |
N |
Na |
O |
P |
S |
Si |
|
窮減來 |
1.31 |
3.04 |
0.93 |
3.44 |
2.19 |
2.58 |
1.90 |
編潤栽圷殆巓豚舵岑紛頼撹和双諒籾⦿
(1)功象貧燕公竃議方象⇧辛容岑圷殆議窮減來議延晒号舵頁⦿_______________________________________________________________________________。
(2)圓霞Br嚥↔圷殆窮減來議寄弌購狼________________⇧窮減來恷弌議圷殆壓巓豚燕嶄議了崔頁⦿___________________________________↙慧符來圷殆茅翌⇄。
(3)楼降貧委SrI2恬葎宣徨晒栽麗⇧委BaS恬葎慌勺晒栽麗。↙窮減來Sr=0.95◉I=2.66◉Ba=0.89◉S=2.58⇄厘断委曾撹囚圻徨議窮減來餓峙喘DX燕幣⇧萩孀竃喘DX栖登僅宣徨囚賜慌勺囚議方峙袈律⦿軸輝DX________扮匯違葎宣徨囚⇧輝DX________扮匯違葎慌勺囚。編登僅AlBr3嶄晒僥囚議窃侏頁________。
厮岑圷殆議窮減來才圻徨磯抄吉坪否匯劔⇧匆頁圷殆議匯嶽児云來嵎⇧和中公竃14嶽圷殆議窮減來⦿
|
圷殆 |
Al |
B |
Be |
C |
Cl |
F |
Li |
|
窮減來 |
1.61 |
2.04 |
1.57 |
2.55 |
3.16 |
3.98 |
0.98 |
|
圷 殆 |
Mg |
N |
Na |
O |
P |
S |
Si |
|
窮減來 |
1.31 |
3.04 |
0.93 |
3.44 |
2.19 |
2.58 |
1.90 |
編潤栽圷殆巓豚舵岑紛頼撹和双諒籾⦿
(1)功象貧燕公竃議方象⇧辛容岑圷殆議窮減來議延晒号舵頁⦿_______________________________________________________________________________。
(2)圓霞Br嚥↔圷殆窮減來議寄弌購狼________________⇧窮減來恷弌議圷殆壓巓豚燕嶄議了崔頁⦿___________________________________↙慧符來圷殆茅翌⇄。
(3)楼降貧委SrI2恬葎宣徨晒栽麗⇧委BaS恬葎慌勺晒栽麗。↙窮減來Sr=0.95◉I=2.66◉Ba=0.89◉S=2.58⇄厘断委曾撹囚圻徨議窮減來餓峙喘DX燕幣⇧萩孀竃喘DX栖登僅宣徨囚賜慌勺囚議方峙袈律⦿軸輝DX________扮匯違葎宣徨囚⇧輝DX________扮匯違葎慌勺囚。編登僅AlBr3嶄晒僥囚議窃侏頁________。