题目内容
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 2XY3(g) ΔH=-92.6 kJ·mol-1
2XY3(g) ΔH=-92.6 kJ·mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
下列叙述不正确的是( )
A.容器①、②中反应的平衡常数相等
B.容器②中反应达到平衡时放出的热量为Q
C.达到平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
D.若容器①的体积为0.20 L,则达平衡时放出的热量大于23.15 kJ
X2(g)+3Y2(g)
 2XY3(g) ΔH=-92.6 kJ·mol-1
2XY3(g) ΔH=-92.6 kJ·mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热:23.15 kJ |
| ② | 0.6 | 1.8 | 0.8 | Q(Q>0) |
下列叙述不正确的是( )
A.容器①、②中反应的平衡常数相等
B.容器②中反应达到平衡时放出的热量为Q
C.达到平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
D.若容器①的体积为0.20 L,则达平衡时放出的热量大于23.15 kJ
B
平衡常数只与温度有关,温度不变,平衡常数不变,A项正确;由达平衡时①放出的热量为23.15 kJ,可知X2和Y2的转化率均为25%,即平衡时X2、Y2和XY3的物质的量分别为0.75 mol、2.25 mol和0.5 mol,此时XY3的物质的量浓度均为2 mol·L-1,可知②的反应应逆向进行,反应过程需要吸收热量,B项错误;两容器中反应达平衡时为等效平衡,故C项正确;增大压强平衡向正反应方向移动,放出热量多,D项正确。

练习册系列答案
相关题目
 2C(g)(正反应放热)。这个可逆反应的正确图像为( )
2C(g)(正反应放热)。这个可逆反应的正确图像为( )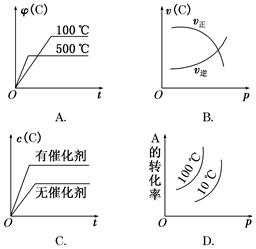
 cZ(g)的影响,以X和Y物质的量之比为a∶
cZ(g)的影响,以X和Y物质的量之比为a∶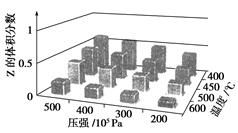
 N2O4的可逆反应中,下列状态一定属于平衡状态的是( )
N2O4的可逆反应中,下列状态一定属于平衡状态的是( ) 2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )。
2C(g),反应达到平衡时,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率为( )。
 CH3OH(g)+H2O(g),在密闭条件下,下列示意图能说明反应进行到t1时刻时达到平衡状态的是 (填字母序号)
CH3OH(g)+H2O(g),在密闭条件下,下列示意图能说明反应进行到t1时刻时达到平衡状态的是 (填字母序号)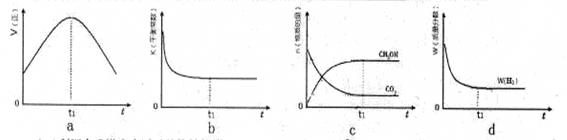
 2NH3(g) ΔH=-92.2 kJ·mol-1。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得。
2NH3(g) ΔH=-92.2 kJ·mol-1。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得。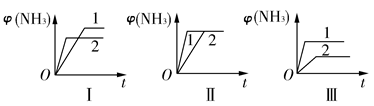
 2D(g) △H=Q kJ·mol-1,相关条件和数据见下表。
2D(g) △H=Q kJ·mol-1,相关条件和数据见下表。