题目内容
下列反应常温时能自发进行,并既能用能量判据又能用熵判据解释的是
| A.HCl(g)+NH3(g)= NH4Cl(s) |
| B.2KClO3(s)=2KCl(s)+3O2(g) |
| C.2Na2O2(s)+2H2O(l)=4NaOH(s)+O2(g) |
| D.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+ 2NH3(g)+10H2O(l) |
C
试题分析:A、该反应是放热反应,常温时能自发进行,但熵值减小,不能用熵判据解释,A不正确;B、氯酸钾分解需要加热,是吸热反应,常温下不能自发进行,不能用能量判据解释,B不正确;C、该反应是放热反应,且是熵值增加的,因此常温下能自发进行,并既能用能量判据又能用熵判据解释,C正确;D、该反应常温下能自发进行,但是吸热反应,不能用能量判据解释,D不正确,答案选C。

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
 4NO2(g)+O2(g) ΔH="+56.7" kJ·mol-1能自发进行的合理解释是( )
4NO2(g)+O2(g) ΔH="+56.7" kJ·mol-1能自发进行的合理解释是( )
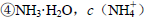 由大到小的顺序是
由大到小的顺序是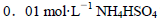 溶液中滴加NaOH溶液至中性:
溶液中滴加NaOH溶液至中性: 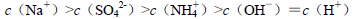

 A(g)+2B(g),已知ΔH<0,下列判断正确的是
A(g)+2B(g),已知ΔH<0,下列判断正确的是 2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大
2NH3(g) △H<0,其他条件不变时,升高温度,反应速率v(H2)和H2的平衡转化率α(H2)均增大