题目内容
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3 + S  Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。
Na2S2O3,常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如右图所示。
Ⅰ.现按如下方法制备Na2S2O3·5H2O:
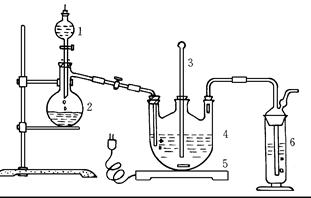
将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按下图安装好装置。
(1)仪器2的名称为 ,
装置6中可放入 。
| A.BaCl2溶液 | B.浓H2SO4 | C.酸性KMnO4溶液 | D.NaOH溶液 |
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二氧化硫气体较均匀的通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,反应原理为:
①Na2CO3+SO2 =Na2SO3+CO2
②Na2S+SO2+H2O=Na2SO3+H2S
③2H2S+SO2=3S↓+2H2O
④Na2SO3+S
 Na2S2O3
Na2S2O3总反应为:2Na2S+Na2CO3+4SO2= 3Na2S2O3+CO2
随着二氧化硫气体的通入,看到溶液中有大量浅黄色固体析出,继续通二氧化硫气体,反应约半小时。当溶液中pH接近或不小于7时,即可停止通气和加热。溶液PH要控制不小于7理由是
(用离子方程式表示)。
Ⅱ.分离Na2S2O3·5H2O并标定溶液的浓度:

(1)为减少产品的损失,操作①为 ,操作②是抽滤洗涤干燥,其中洗涤操作是用
(填试剂)作洗涤剂。
(2)蒸发浓缩滤液直至溶液呈微黄色浑浊为止,蒸发时为什么要控制温度不宜过高
(3)称取一定质量的产品配置成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准
确称取基准物质K2Cr2O7(摩尔质量294g/mol)0.5880克。平均分成3份分别放入3个锥形瓶中,加
水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+=3I2+2Cr3++7H2O,再加入几滴
淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,滴定终点的现象为
三次消耗Na2S2O3溶液的平均体积为20.00mL,则所标定的硫代硫酸钠溶液
的浓度为 mol/L。
(15分) Ⅰ.(1)蒸馏烧瓶(1分),CD(2分,选对一个1个1分,答错不给分)
(2)S2O32-+2H+=S↓+SO2↑+H2O(2分)
Ⅱ.(1)趁热过滤(2分,写过滤得1分),乙醇(1分) (2)温度过高会导致析出的晶体分解(2分)
(3)溶液由蓝色恰好变成无色,且半分钟不恢复(2分)0.2000(3分)
解析试题分析:Ⅰ.(1)根据仪器的构造可知,仪器2的名称为蒸馏烧瓶;由于实验中有SO2生成,而SO2是大气污染物,不能随意排放,需要尾气处理。随意装置6的作用是吸收SO2,防止污染空气。SO2是酸性氧化物,且具有还原性,所以可用酸性高锰酸钾溶液或氢氧化钠溶液吸收,答案选CD。
(2)因为在酸性条件下,硫代硫酸钠易生成SO2、S和水,反应的离子方程式是S2O32-+2H+=S↓+SO2↑+H2O。
Ⅱ.(1)由于硫代硫酸钠的溶解度随温度的升高而降低,所以操作I应该是趁热过滤;;Na2S2O3易溶于水,不溶于乙醇,所以为防止洗涤损失硫代硫酸钠,应该用乙醇作洗涤剂。
(2)由于Na2S2O3·5H2O于40~45℃熔化,48℃分解,所以蒸发时要控制温度不宜过高的原因是温度过高会导致析出的晶体分解。
(3)由于碘遇淀粉显蓝色,所以滴定终点的现象为溶液由蓝色恰好变成无色,且半分钟不恢复;根据反应的方程式可知:K2Cr2O7~3I2~6 Na2S2O3
1mol 6mol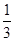 ×0.5880g÷294g/mol c×0.02000L
×0.5880g÷294g/mol c×0.02000L
解得c=0.2000mol/L
考点:考查仪器的识别、尾气处理;实验条件的控制;滴定实验操作以及物质的量浓度的测定和计算等

 阅读快车系列答案
阅读快车系列答案下列说法正确的是
| A.在“食醋总酸含量的测定”实验中,选择酚酞溶液为指示剂,当溶液的颜色变为粉红色且在半分钟内不褪色,即达到滴定终点 |
| B.在“牙膏中某些主要成分的检验”实验中,在牙膏与蒸馏水搅拌、静置分离后的澄清溶液中加入少量的新制Cu(OH)2,当产生绛蓝色沉淀时,说明牙膏中含有甘油 |
| C.在“阿司匹林的合成”实验中,把从盐酸中析出的晶体进行抽滤,用酒精洗涤晶体1~2次,然后抽滤,将晶体转移到表面皿上,干燥后称其质量,计算产率。 |
| D.人体吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合蒸气解毒;氨气、溴中毒休克时要马上进行人工呼吸 |
下列叙述正确的是
| A.用湿润的pH试纸测溶液的pH |
| B.用蒸馏法可将海水淡化为可饮用水 |
| C.常温下浓硫酸不能盛放在铝制容器中 |
| D.配制溶液时仰视容量瓶刻度线定容会使溶液浓度偏高 |
下列根据实验操作及现象所得出的结论中,正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向两份蛋白质溶液中分别滴加NaCl溶液和 CuSO4溶液。均有固体析出 | 蛋白质均发生了变性 |
| B | 取少量Fe(NO3)2试样加水溶解,加稀硫酸酸化, 滴‘加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经 变质 |
| C | 将少量某物质的溶液滴加到新制的银氨溶液中, 水浴加热后有银镜生成 | 该物质一定属于醛类 |
| D | 同条件下,分别将0.1mol·L-1的盐酸和醋酸进 行导电性实验,与醋酸串联的灯泡较暗 | 醋酸是弱酸 |
下列实验装置不能达到实验目的的是
| A.甲装置电解精炼铝 | B.乙装置制备Fe(OH)2 |
| C.丙装置可得到金属铁 | D.丁装置验证NaHCO3和Na2CO3的热稳定性 |
下列说法不正确的是
| A.漂白粉长时间露置空气中会结块变质 |
| B.把NaHSO4溶液加入NaAlO2中生成白色沉淀然后沉淀又溶解 |
| C.装强碱溶液的试剂瓶需要用橡胶塞,长时间后会在瓶口有白色固体生成 |
| D.蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生 |
下列实验现象或结论错误的是
| 选项 | 实 验 | 现象或结论 |
| A | 取少量某溶液,滴加过量的稀盐酸无明显现象,再滴加BaCl2溶液 | 出现白色沉淀,则该溶液中含有SO42- |
| B | 相同温度下,取两份等质量的锌粒分别与足量稀酸反应,向其中一份中加入几滴CuSO4溶液 | 加入ZnSO4溶液的产生氢气快,最终二者生成氢气的量相同 |
| C | 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 | 反应速率:粉状大理石>块状大理石 |
| D | 向Na2S溶液中滴入ZnSO4溶液有白色沉淀生成,再加入几滴ZnSO4溶液 | 沉淀由白色转化为黑色,说明溶度积(Ksp):ZnS>CuS |
