题目内容
在25℃ 101kPa下,白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程式分别为
P4(s)+5O2(g)= P4O10(s);△H = -3093.2 kJ/mol,
4P(s)+5O2(g)= P4O10(s);△H = -2954.0 kJ/mol,
由此判断,下列说法正确的是
P4(s)+5O2(g)= P4O10(s);△H = -3093.2 kJ/mol,
4P(s)+5O2(g)= P4O10(s);△H = -2954.0 kJ/mol,
由此判断,下列说法正确的是
[ ]
A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高
B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低
C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高
D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低
B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低
C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高
D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低
D

练习册系列答案
相关题目
下列有关化学用语正确的是( )
A、氧的原子结构示意图为: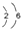 | B、用电子式表示水分子形成的过程为: | C、11.2L氢气在25℃101kPa下燃烧,生成液态的水放出285.8kJ的热量,则该反应的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ/mol | D、氢氧化铝电离方程式为:Al(OH)3?Al3++3OH- |
下列有关化学用语表示正确的是
A.S2-的结构示意图: |
| B.原子核内有10个中子,8个质子的原子:18 8O |
| C.HSO3-的电离方程式:HSO3-= H++SO32- |
| D.2gH2在25℃101kPa下燃烧,生成液态的水放出285.8kJ·mol-1的热量,则该反应的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ·mol-1 |