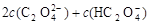题目内容
10.草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol/L NaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是A.V(NaOH)=0时,c(H+)=1×10-2 mol/L
B.V(NaOH)<10 mL时,不可能存在c(Na+)=![]()
C.V(NaOH)=10 mL时,c(H+)=1×10-7 mol/L
D.V(NaOH)>10 mL时,![]()
D
解析:本题以中和滴定为载体考查考生对溶液中各离子浓度的大小关系的比较方法的掌握程度。由于草酸为二元中强酸,故HC2O![]() 不能完全电离产生H+,所以V(NaOH)=0时,c(H+)<10-2 mol·L-1,A项不正确;根据电荷守恒关系有c(H+)+c(Na+)=2c(C2O
不能完全电离产生H+,所以V(NaOH)=0时,c(H+)<10-2 mol·L-1,A项不正确;根据电荷守恒关系有c(H+)+c(Na+)=2c(C2O![]() )+c(HC2O
)+c(HC2O![]() )+c(OH-),当V(NaOH)=10 mL时,NaHC2O4与NaOH恰好完全反应,因C2O
)+c(OH-),当V(NaOH)=10 mL时,NaHC2O4与NaOH恰好完全反应,因C2O![]() 水解而呈碱性,C项不正确;当V(NaOH)<10 mL而c(H+)=c(OH-)时,由上述关系知B项不正确;由于C2O
水解而呈碱性,C项不正确;当V(NaOH)<10 mL而c(H+)=c(OH-)时,由上述关系知B项不正确;由于C2O![]() 的水解是微弱的,故当V(NaOH)>10 mL时,c(Na+)>c(C2O
的水解是微弱的,故当V(NaOH)>10 mL时,c(Na+)>c(C2O![]() )>c(HC2O
)>c(HC2O![]() )的关系正确。
)的关系正确。

练习册系列答案
相关题目
草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol/L NaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH)="=" 0时,c(H+,W)="=" 1 × 10-2 mol/L |
B.V(NaOH)< 10 mL时,不可能存在c(Na+)="=" 2 c(C2O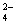 )+ c(HC2O )+ c(HC2O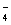 ) ) |
| C.V(NaOH)="=" 10 mL时,c(H+,W)="=" 1 × 10-7mol/L |
D.V(NaOH)> 10 mL时,c(Na+)> c(C2O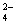 )>c(HC2O )>c(HC2O ) ) |