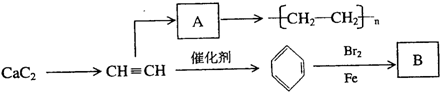
题目内容
如图为实验室制取乙炔并验证其性质的装置图.下列说法不合理的是( )
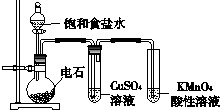

| A、逐滴加入饱和食盐水可控制生成乙炔的速率 | B、KMnO4酸性溶液褪色,说明乙炔具有还原性 | C、用Br2的CCl4溶液验证乙炔的性质,不需要除杂 | D、将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高 |
分析:A、逐滴加入饱和食盐水时可控制反应物水的供给,从而控制生成乙炔的速率;
B、酸性KMnO4溶液能氧化乙炔,所以乙炔使酸性KMnO4溶液褪色;
C、乙炔气体中混有的硫化氢可以被Br2氧化,对乙炔性质的检验产生干扰;
D、对于烃类物质而言,不饱和程度越高,则含碳量越高,火焰越明亮,冒出的烟越浓.
B、酸性KMnO4溶液能氧化乙炔,所以乙炔使酸性KMnO4溶液褪色;
C、乙炔气体中混有的硫化氢可以被Br2氧化,对乙炔性质的检验产生干扰;
D、对于烃类物质而言,不饱和程度越高,则含碳量越高,火焰越明亮,冒出的烟越浓.
解答:解:A、电石跟水反应比较剧烈,所以用饱和食盐水代替水,逐滴加入饱和食盐水时可控制反应物水的供给,从而控制生成乙炔的速率,故A正确;
B、酸性KMnO4溶液能氧化乙炔,因此乙炔使酸性KMnO4溶液褪色,表现了乙炔的还原性,故B正确;
C、乙炔气体中混有的硫化氢可以被Br2氧化,对乙炔性质的检验产生干扰,所以应用硫酸铜溶液洗气,故C错误;
D、对于烃类物质而言,不饱和程度越高,则含碳量越高,火焰越明亮,冒出的烟越浓,乙炔含有碳碳三键,是不饱和程度较高的烃类物质,故D正确;
故选:C.
B、酸性KMnO4溶液能氧化乙炔,因此乙炔使酸性KMnO4溶液褪色,表现了乙炔的还原性,故B正确;
C、乙炔气体中混有的硫化氢可以被Br2氧化,对乙炔性质的检验产生干扰,所以应用硫酸铜溶液洗气,故C错误;
D、对于烃类物质而言,不饱和程度越高,则含碳量越高,火焰越明亮,冒出的烟越浓,乙炔含有碳碳三键,是不饱和程度较高的烃类物质,故D正确;
故选:C.
点评:本题考查乙炔气体的制备原理、装置和注意事项,其中注意事项非常重要,均可设计成该气体制备实验的考点,整体难度不大,C为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
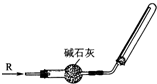
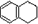 ,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
,分子式是C10H12.常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2→C10H8Br4+4HBr.生成的四溴化萘常温下为固态,不溶于水,有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,实验步骤如下:
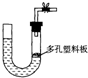
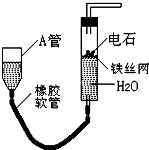 如图的实验装置可用于实验室中制取乙炔.请回答下列问题:
如图的实验装置可用于实验室中制取乙炔.请回答下列问题: