题目内容
将3.9g镁铝合金,投入到500mL 2mol·L-1的盐酸中,金属完全溶解,再加入4mol·
L-1的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是
A.125mL B.200mL C.250mL D.560mL
【答案】
C
【解析】
试题分析:当沉淀达到最大值时,溶液中的溶质就是氯化钠,所以根据原子守恒可知:n(NaOH)=n(HCl),则氢氧化钠溶液的体积是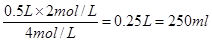 ,答案选C。
,答案选C。
考点:考查镁铝合金溶于酸的有关计算
点评:该题是基础性试题的考查,也是高考中的常见考点。该题的关键是判断出溶液中的溶质,然后借助于原子守恒列式就是即可,学生不难得分。

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
将3.9g镁铝合金,投入到500mL 2mol/L的盐酸中,合金完全溶解,再加入5mol/L的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是( )
| A、100mL | B、150mL | C、200mL | D、250mL |
将3.9g镁铝合金,投入到500mL 2mol/L的盐酸中,合金完全溶解,再加入5mol/L的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是( )
| A、125mL | B、200mL | C、250mL | D、560mL |
将3.9g镁铝合金投入到500mL2mol·L-1的盐酸中,金属完全溶解,再加入4mol·L-1的NaOH溶液,若要生成的沉淀最多,加入NaOH溶液的体积是( )
| A.125mL | B.200mL | C.250mL | D.560mL |