题目内容
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂之一。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为 (反应①)。
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应化学方程式为 (反应②)。
(3)次氯酸不稳定,容易分解,化学反应方程式为 (反应③)。
(4)反应①、反应②、反应③中,属于氧化还原反应的是(填反应编号) 。
(1)2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
(2)Ca(ClO)2+CO2+H2O=CaCO3+2HClO
(3)2HClO=2HCl+O2↑
(4)①,③
解析试题分析:(1)氯气与碱发生歧化反应,生成氯化钙和次氯酸钙,然后根据得失电子守恒配平即可。书写方程式时也可以看作氯气先与水反应生成盐酸和次氯酸,然后酸再和碱发生中和反应。
(2)根据强酸制弱酸的原理,碳酸的酸性大于次氯酸,所以Ca(ClO)2+CO2+H2O=CaCO3+2HClO
(3)次氯酸不稳定,见光分解为HCl和O2。
(4)有元素化合价升降的反应是氧化还原反应。反应②中元素化合价没有发生变化。
考点:考查漂白粉的制备和漂白原理。

练习册系列答案
相关题目
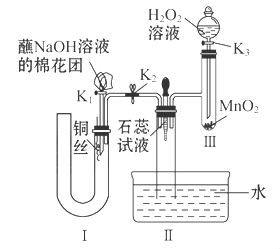
硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。
Ⅰ、硬质玻璃管常作为气体和固体反应的场所,如图(其他装置省略,必要时可加热)。
下列实验描述不正确的是
| A.固体A为无水硫酸铜时,可以检验气体X中是否含有水蒸气 |
| B.固体A为铜时,可以除去N2中的O2 |
| C.在空气流作用下,加热氯化铁晶体得到纯净的无水氯化铁 |
| D.将氨气和空气混合气通过灼热的铂丝,可看到有红棕色气体生成 |
a、b、c三个棉球变化如下表。请填写表中的空白:
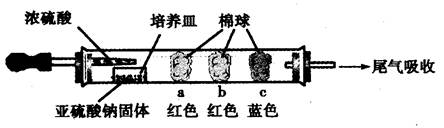
| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
| a | | 棉球变白,微热后又恢复红色 | |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
| c | | 棉球变为白色 | 结论:该气体具有 性 |