题目内容
12.下列离子方程式与所述事实相符且正确的是( )| A. | 铝和氢氧化钠溶液反应:2Al+2OH-=2AlO2-+H2↑ | |
| B. | 铜与足量FeCl3溶液反应:Fe3++Cu=Fe2++Cu2+ | |
| C. | 用醋酸除去水瓶中的水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | 向苯酚钠溶液中通入CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- |
分析 A.原子个数不守恒;
B.电荷不守恒;
C.醋酸为弱电解质,应保留化学式;
D.苯酚钠溶液与二氧化碳反应生成苯酚和碳酸氢钠.
解答 解:A.铝和氢氧化钠溶液反应,离子方程式:2Al+20H-+H2O=2Al02-+3H2↑,故A错误;
B.铜与足量FeCl3溶液反应,离子方程式:2Fe3++Cu=2Fe2++Cu2+,故B错误;
C.用醋酸除去水瓶中的水垢,离子方程式:CaCO3+2CH3COOH=Ca2++H2O+CO2↑2CH3COO-,故C错误;
D.向苯酚钠溶液中通入CO2,离子方程式:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确书写方法,注意电荷守恒、原子个数守恒、化学式拆分即可解答,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
20.下列叙述中不正确的是( )
| A. | 电能是二级能源 | B. | 水力是一级能源 | ||
| C. | 煤、石油、天然气是一级能源 | D. | 水煤气是一级能源 |
4.X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大.有关信息如下表:
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式: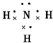 .
.
(2)已知37Rb和53I都位于第五周期,分别与Z和M位于同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式:8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
| X | 动植物生产不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正价与负价的代数和为6 |
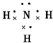 .
.(2)已知37Rb和53I都位于第五周期,分别与Z和M位于同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式:8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
16.已知短周期元素的离子:aA2+、bB+、cC2-、dD-具有相同的电子层结构,则下列说法正确的是( )
| A. | A元素与C元素在同一周期 | B. | 原子半径:A>B>C>D | ||
| C. | b=d+2 | D. | 离子半径:D->C2->B+>A2+ |
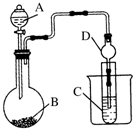 某化学兴趣小组利用如图装置验证元素非金属性的变化规律.
某化学兴趣小组利用如图装置验证元素非金属性的变化规律.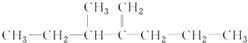 ,此烃名称为3-甲基-2-丙基-1-戊烯.
,此烃名称为3-甲基-2-丙基-1-戊烯.