题目内容
在密闭容器中进行如下反应:X2(g)+Y2(g)![]() 2Z(g)
2Z(g)
已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
A.Z为0.3 mol·L-1 B.Y2为0.35 mol·L-1
C.X2为0.2 mol·L-1 D.Z为0.4 mol·L-1
解析:(1)假设反应向右进行到底
X2(g) + Y2(g) ![]() 2Z(g)
2Z(g)
始/mol·L-1 0.1 0.3 0.2
变/mol·L-1 0.1 ?=0.1 ?=0.2
终/mol·L-1 ??=0 ??=0.2 ??=0.4
(2)假设反应向左进行到底
X2(g) + Y2(g)![]() 2Z(g)
2Z(g)
始/mol·L-1 0.1 0.3 0.2
变/mol·L-1 0.1 ?=0.1 0.2
终/mol·L-1 ??=0.2 ??=0.4 ??=0
可逆进行不到底,各物质的平衡浓度介于上述两种极端情况之间。据此即可判断各物质能否达到选项中的浓度。
答案:AB

练习册系列答案
相关题目
在密闭容器中进行如下反应:X(g)+Y(g)?2Z(g),已知X、Y、Z的起始浓度分别为0.1mol/L、0.2mol/L、0.2mol/L,在一定条件下,达到平衡时,各物质的浓度不可能是( )
| A、Z为0.3 mol/L | B、Y为0.15 mol/L | C、X为0.1 mol/L | D、Z为0.4 mol/L |
在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )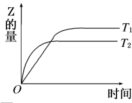

| A、T1<T2,正反应是放热反应 | B、T1<T2,正反应是吸热反应 | C、T1>T2,正反应是放热反应 | D、T1>T2,正反应是吸热反应 |
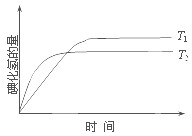 在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g);△H,在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )
在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g);△H,在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )