题目内容
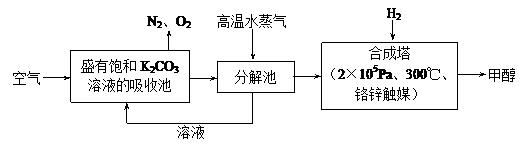
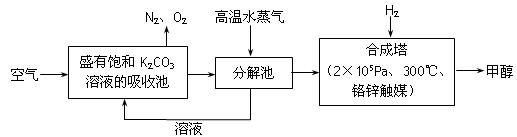
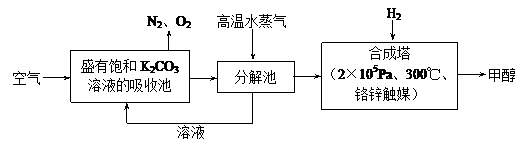
为减小和消除由于操作原因CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下
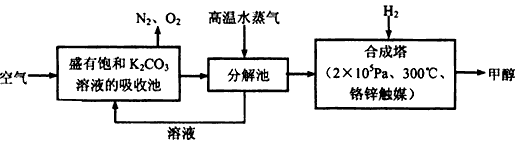
(1)在合成塔中,若有4.4 kg CO2与足量H2恰好完全反应,可放出4947 kJ的热量,试写出合成塔中发生反应的热化学方程式是_____________________。
(2)以甲醇为燃料制作新型燃料电池,电池的正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是:CH3OH+H2O-6e-=CO2+6H+,则正极发生的反应是__________________;放电时,H+移向电池的____(填“正”或“负”)极。
(3)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3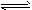 HCO3-+H+的平衡常数 K=____。(已知:10-5.6=2.5×10-6)
HCO3-+H+的平衡常数 K=____。(已知:10-5.6=2.5×10-6)
(4)常温下,0.1mol·L-1 NaHCO3溶液的pH大于8,则溶液中c(H2CO3)______ (填“>”“=”或“<”)
c(CO32-),原因是___________________ (用离子方程式和必要的文字说明)。
(5)小李同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp分别为
4. 96×10-9、2.58×10-9)小李应该选用的试剂是________
(2)以甲醇为燃料制作新型燃料电池,电池的正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是:CH3OH+H2O-6e-=CO2+6H+,则正极发生的反应是__________________;放电时,H+移向电池的____(填“正”或“负”)极。
(3)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3
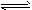 HCO3-+H+的平衡常数 K=____。(已知:10-5.6=2.5×10-6)
HCO3-+H+的平衡常数 K=____。(已知:10-5.6=2.5×10-6) (4)常温下,0.1mol·L-1 NaHCO3溶液的pH大于8,则溶液中c(H2CO3)______ (填“>”“=”或“<”)
c(CO32-),原因是___________________ (用离子方程式和必要的文字说明)。
(5)小李同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp分别为
4. 96×10-9、2.58×10-9)小李应该选用的试剂是________
(1)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=-49.47 kJ/mol
(2)O2+4H++4e-=2H2O;正
(3)4.2×10-7 mol/L
(4) 因为既存在HCO3-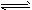 CO32-+H+也存在HCO3-+H2O
CO32-+H+也存在HCO3-+H2O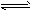 H2CO3+OH-,而HCO3-的水解程度大于电离程度
H2CO3+OH-,而HCO3-的水解程度大于电离程度
(5)Ba(OH)2溶液(或NaOH溶液和BaCl2溶液)
(2)O2+4H++4e-=2H2O;正
(3)4.2×10-7 mol/L
(4) 因为既存在HCO3-
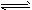 CO32-+H+也存在HCO3-+H2O
CO32-+H+也存在HCO3-+H2O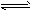 H2CO3+OH-,而HCO3-的水解程度大于电离程度
H2CO3+OH-,而HCO3-的水解程度大于电离程度(5)Ba(OH)2溶液(或NaOH溶液和BaCl2溶液)

练习册系列答案
相关题目