题目内容
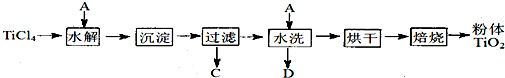
TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。某学习小组同学在实验室用钛铁矿精矿(主要成分为FeTiO3及少量SiO2等杂质)模拟工业生产TiO2, 设计流程如下
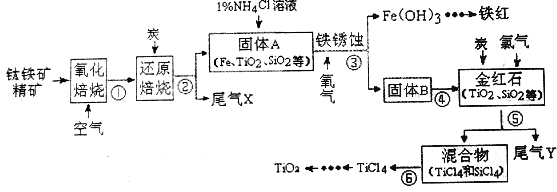
回答下列问题:
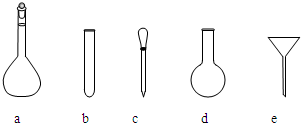
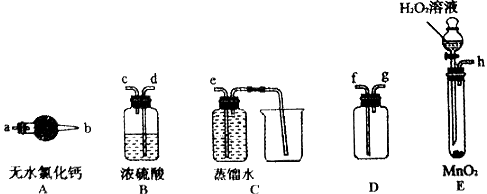
(1)选择必要的装置制备并收集干燥、纯净的氧气,按气流方向装置的正确连接顺序为_________________ (填仪器接口的字母编号);检查装置E气密性的操作过程为___________。
(1)选择必要的装置制备并收集干燥、纯净的氧气,按气流方向装置的正确连接顺序为_________________ (填仪器接口的字母编号);检查装置E气密性的操作过程为___________。
(2)步骤③铁发生电化学腐蚀的过程中,O2除参与电极反应外,还参与另外一个化学反应,该反应的化学方程式为_________________
(3)步级④中固体B经过洗涤得到金红石,验证金红石Cl–己洗净的实验方法是____________
(4)步骤⑤中产生的尾气Y中含有少量Cl2会污染环境,下列可用于吸收Cl2的试剂为_______(填字母序号) .
a.饱和食盐水 b.浓硫酸 c.浓NaOH溶液 d.石灰乳
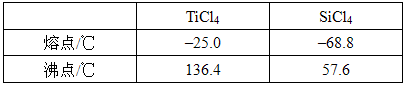
(5)分析下表数据,步骤⑥中分离TiCl4和SiCl4混合物的操作名称为_______,所用到的主要玻璃仪器除酒精灯、温度计外还有________________。
(3)步级④中固体B经过洗涤得到金红石,验证金红石Cl–己洗净的实验方法是____________
(4)步骤⑤中产生的尾气Y中含有少量Cl2会污染环境,下列可用于吸收Cl2的试剂为_______(填字母序号) .
a.饱和食盐水 b.浓硫酸 c.浓NaOH溶液 d.石灰乳
(5)分析下表数据,步骤⑥中分离TiCl4和SiCl4混合物的操作名称为_______,所用到的主要玻璃仪器除酒精灯、温度计外还有________________。
(1)hdcfgab(或hdcfg或habfg);用导管连接h,将导管末端浸入盛水的水槽中,关闭分液漏斗的活塞,用手捂热试管,若导管口有气泡冒出,且松手一段时间后,导管中有水回流形成一段稳定的液柱,证明气密性良好
(2)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(3)去最后一次洗涤液,向其滴加硝酸酸化的硝酸银溶液,无白色沉淀形成,证明Cl–已洗净
(4)cd
(5)蒸馏;蒸馏烧瓶、冷凝管、牛角管、锥形瓶
(2)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(3)去最后一次洗涤液,向其滴加硝酸酸化的硝酸银溶液,无白色沉淀形成,证明Cl–已洗净
(4)cd
(5)蒸馏;蒸馏烧瓶、冷凝管、牛角管、锥形瓶

练习册系列答案
相关题目

 TiO2?xH2O↓+4HCl
TiO2?xH2O↓+4HCl