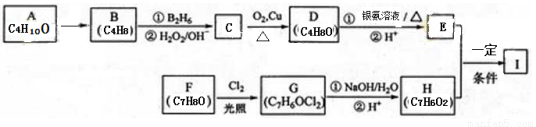
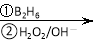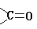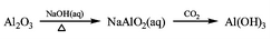题目内容
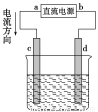
关于下列装置说法正确的是
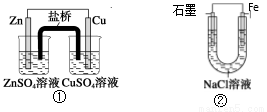
A.装置①中,盐桥中的K+移向CuSO4溶液
B.装置①中,Zn为负极,发生还原反应
C.装置②中的Fe发生析氢腐蚀
D.装置②中电子由Fe流向石墨,然后再经溶液流向Fe
A
【解析】
试题分析:A.装置①为原电池反应。Zn作负极,Cu作正极。根据同种电荷相互排斥,异种电荷相互吸引的原则,盐桥中的K+移向负电荷较多的正极一方,即盛有CuSO4溶液的烧杯中。正确。B.装置①中,Zn为负极,发生氧化反应Zn-2e-=Zn2+。错误。C.在装置②的原电池反应中。由于NaCl溶液是中性溶液,所以其中的Fe发生的是吸氧腐蚀。错误。D.活动性Fe大于C,所以Fe失去电子,作负极,电子经导线流向石墨,然后在正极C上发生还原反应O2+4e-+2H2O=4OH-。在溶液中,Na+向C电极移动,Cl-向Fe电极移动。形成闭合回路。错误。
考点:考查原电池中的电极反应及电子流动、电荷移动的问题的知识。

A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Ag+ Na+ |
阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27g。常温下各烧杯中溶液的pH与电解时间(t)的关系如图。据此回答下列问题:
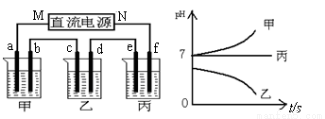
(1)M为电源的 极(填“正”或“负”),甲电解质为 (填化学式)。
(2)写出丙烧杯中反应的化学方程式 。
(3)有人设想用图一所示原电池为直流电源完成上述电解。则锌电极相当于直流电源的 (填“M”或“N”)极。
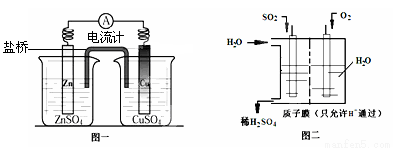
(4)有人设想用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化
为重要化工原料。该设想中负极的电极反应式为 。
现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性; C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 (用离子方程式表示)。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子
浓度 倍。
(4)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或-1)
浓度由大到小的顺序为: 。