题目内容
工业上为了处理含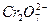 离子的酸性废水,采用以下处理方法:
离子的酸性废水,采用以下处理方法:
①往工业废水中加入适量食盐。
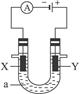
②以铁作为阳极进行电解。
③鼓入空气。经过一段时间后,使废水中含铬量降到可排放的标准。
请用已学过的化学知识解释处理含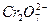 离子的工业废水的原因。
离子的工业废水的原因。
注:Fe(OH)3开始沉淀的pH为2.7,沉淀完全的pH为3.7。Fe(OH)2开始沉淀的pH为7.6,沉淀完全的pH为9.6,并且Fe(OH)2呈絮状沉淀,不易从溶液中除去。
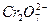 离子的酸性废水,采用以下处理方法:
离子的酸性废水,采用以下处理方法:①往工业废水中加入适量食盐。
②以铁作为阳极进行电解。
③鼓入空气。经过一段时间后,使废水中含铬量降到可排放的标准。
请用已学过的化学知识解释处理含
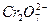 离子的工业废水的原因。
离子的工业废水的原因。注:Fe(OH)3开始沉淀的pH为2.7,沉淀完全的pH为3.7。Fe(OH)2开始沉淀的pH为7.6,沉淀完全的pH为9.6,并且Fe(OH)2呈絮状沉淀,不易从溶液中除去。
选择以铁做阳极:以Fe为阳极,电极反应式为:
阳极: Fe-2e-====Fe2+ 阴极: 2H++2e-====H2↑
加入少量食盐,是增加污水中离子浓度,增强导电能力。以生成的Fe2+为还原剂,在酸性溶液中与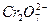 离子发生氧化还原反应,离子方程式略。
离子发生氧化还原反应,离子方程式略。
这样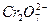 被还原成Cr3+。在电解过程中,由于H+在阴极不断放电,打破了水的电离平衡、促进水的电离,溶液的pH上升,溶液中的阳离子以Cr(OH)3、Fe(OH)2、Fe(OH)3形成沉淀。
被还原成Cr3+。在电解过程中,由于H+在阴极不断放电,打破了水的电离平衡、促进水的电离,溶液的pH上升,溶液中的阳离子以Cr(OH)3、Fe(OH)2、Fe(OH)3形成沉淀。
由信息可知,Fe(OH)2开始沉淀的pH为7.6,沉淀完全的pH为9.6,并且Fe(OH)2呈絮状沉淀不便分离,不易从溶液中除去。根据已学的知识,Fe(OH)2极易被O2氧化,所以在处理过程中鼓入空气,让空气中O2充分与Fe(OH)2反应(反应方程式略),成为容易分离的Cr(OH)3、Fe(OH)3,使废水含铬量降到可排放标准。
阳极: Fe-2e-====Fe2+ 阴极: 2H++2e-====H2↑
加入少量食盐,是增加污水中离子浓度,增强导电能力。以生成的Fe2+为还原剂,在酸性溶液中与
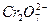 离子发生氧化还原反应,离子方程式略。
离子发生氧化还原反应,离子方程式略。这样
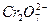 被还原成Cr3+。在电解过程中,由于H+在阴极不断放电,打破了水的电离平衡、促进水的电离,溶液的pH上升,溶液中的阳离子以Cr(OH)3、Fe(OH)2、Fe(OH)3形成沉淀。
被还原成Cr3+。在电解过程中,由于H+在阴极不断放电,打破了水的电离平衡、促进水的电离,溶液的pH上升,溶液中的阳离子以Cr(OH)3、Fe(OH)2、Fe(OH)3形成沉淀。由信息可知,Fe(OH)2开始沉淀的pH为7.6,沉淀完全的pH为9.6,并且Fe(OH)2呈絮状沉淀不便分离,不易从溶液中除去。根据已学的知识,Fe(OH)2极易被O2氧化,所以在处理过程中鼓入空气,让空气中O2充分与Fe(OH)2反应(反应方程式略),成为容易分离的Cr(OH)3、Fe(OH)3,使废水含铬量降到可排放标准。
本题重点探讨以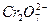 为污染源的工业污水处理法。涉及到的化学知识:
为污染源的工业污水处理法。涉及到的化学知识:
①对氧化—还原反应,电解池的原理的理解和应用、电解池的电极分为惰性电极和金属电极。
②电解过程中溶液pH的变化以及pH变化对沉淀的影响。
③廉价化工原料的选择,不断鼓入空气的原因。
④离子方程式的书写。
⑤物质分离方法的选择。
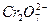 为污染源的工业污水处理法。涉及到的化学知识:
为污染源的工业污水处理法。涉及到的化学知识:①对氧化—还原反应,电解池的原理的理解和应用、电解池的电极分为惰性电极和金属电极。
②电解过程中溶液pH的变化以及pH变化对沉淀的影响。
③廉价化工原料的选择,不断鼓入空气的原因。
④离子方程式的书写。
⑤物质分离方法的选择。

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
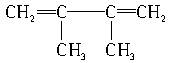 和y mol CH2==CH—CN经加聚形成高聚物A,A在适量的氧气中完全燃烧生成二氧化碳、水蒸气和氮气,其中二氧化碳占总体积的52.6%,则x∶y约是( )
和y mol CH2==CH—CN经加聚形成高聚物A,A在适量的氧气中完全燃烧生成二氧化碳、水蒸气和氮气,其中二氧化碳占总体积的52.6%,则x∶y约是( )