题目内容
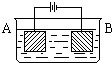 某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液.通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为( )
某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液.通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为( )分析:原理中A上有多少Cu溶解,同时B上就有同样多的Cu析出,而A中Zn溶解,以Zn2+进入溶液,同时Cu2+在B极上析出,电子是守恒的,此过程会导致溶液质量增加,设A合金中Cu的物质的量为x,Zn的物质的量为y,结合反应的方程式计算.
解答:解:因为A极是铜锌合金,溶液为足量的硫酸铜溶液,A极恰好全部溶解,所以当锌溶解时,B极照样析出铜,因为锌离子和铜离子都为+2价,设A合金中Cu的物质的量为x,Zn的物质的量为y,
则
解得x=0.06,y=0.03,
则合金中Cu、Zn原子个数比为0.06:0.03=2:1,
故选C.
则
|
解得x=0.06,y=0.03,
则合金中Cu、Zn原子个数比为0.06:0.03=2:1,
故选C.
点评:本题考查电解原理,侧重于电解的计算,注意把握两极的变化,从守恒的角度解答该题,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
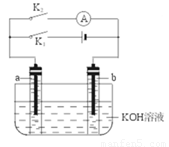
 (2008?梅州一模)如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )
(2008?梅州一模)如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法不正确的是( )