题目内容
|
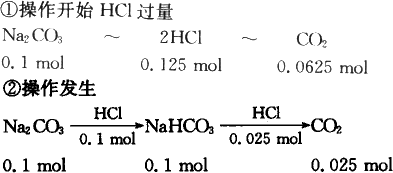
①将0.1 L 1 mol·L-1的纯碱溶液逐滴滴入0.1 L 1.25 mol·L-1的盐酸中;②将0.1 L 1.25 mol·L-1的盐酸逐滴滴入到0.1 L 1 mol·L-1的纯碱溶液中,两种操作产生CO2的体积比为 | |
| [ ] | |
A. |
5∶2 |
B. |
2∶5 |
C. |
2∶1 |
D. |
1∶1 |
解析:
|
|

 备战中考寒假系列答案
备战中考寒假系列答案|
①将 0.1 L 1mol/L纯碱溶液逐滴滴到0.1 L 1.25 mol/L盐酸中;②将0.1 L 1.25 mol/L盐酸逐滴滴到0.1 L 1 mol/L纯碱溶液中.两种操作产生CO2的体积比为 | |
| [ ] | |
A. |
5∶2 |
B. |
2∶5 |
C. |
2∶1 |
D. |
1∶1 |
(10分)已知金属镁与氯化铁和氯化铜溶液反应有多种实验假设。甲、乙两位同学分别设计合理实验步骤探究该反应的历程。
提出猜想:
甲:推测镁与氯化铁、氯化铜水解产生中的H+反应,拉动水解平衡生成生成H2。
乙:推测镁应与氯化铁、氯化铜发生氧化还原反应。
结合对试剂的选择两位同学做了如下实验:
实验过程
编号 | 实验操作 | 预期现象和结论 |
① | 将打磨过的镁条取加入经盐酸酸化的饱和氯化铁溶液,充分反应 | 始终有大量气泡,颜色无明显变化,未见沉淀生成反应完全后取出镁条发现可被磁铁吸引 |
② | 将打磨过的镁条取加入0.1mol/L氯化铁溶液,充分反应 | 有少量气泡,颜色变浅,有红褐色沉淀生成,反应完全后取出镁条发现不能被磁铁吸引 |
根据实验操作,实验现象,甲、乙分别推测解释相应的结论。
(1)写出生成Fe(OH)3胶体的离子方程式:
(2)与甲同学的推测不尽符合的现象是 ,
在实验①③的基础上甲进一步提出猜测:镁与H+反应拉动饱和氯化铁的水解平衡生成Fe(OH)3胶体,故未看到沉淀现象。
要验证甲的进一步猜想,还须补做的实验是
提出你的猜想
(3)乙:根据实验②可推测
(4)结合甲,乙两位同学的推测,你能否谈谈对上述实验事实的认识:
![]()
实验室通过实验测定NaOH溶液和盐酸反应的中和热.实验需用约450mL 0.50mol/L NaOH溶液.容量瓶(100mL,250mL,500mL各一个)
(1)配制0.50 mol/L NaOH溶液:将NaOH固体放在 (填实验用品或仪器的名称),用托盘天平 g NaOH固体.在使用容量瓶前必须进行的操作是
.
(2)下列操作会使所配溶液的浓度偏高的是(填序号) .
A.烧杯、玻璃棒没有洗涤
B.转移时有溶液溅出容量瓶外
C.定容时,将容量瓶上、下颠倒摇匀后发现液面低于刻度线再加水
D.容量瓶用蒸馏水洗涤后再用相同溶质的溶液润洗
E.定容时俯视容量瓶刻度线.
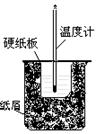
(3)将50mL 0.50mol/L盐酸与60mL 0.50mol/L NaOH溶液在右图所示
的装置中进行中和反应.从实验装置上看,图中尚缺少的一种玻
|
(4)一定量的稀盐酸和过量的NaOH溶液反应,当生成1mol H2O时放出的热量为57.3 kJ,则该反应的热化学方程式为 .
已知:① HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l);△H=-a kJ·mol-1
② HCl(aq)+NaOH(s)=NaCl(aq)+H2O(l);△H=-b kJ·mol-1
③ HNO3(aq)+KOH(aq)=NaNO3(aq)+H2O(l);△H=-c kJ·mol-1
则a、b、c三者的大小关系为 (填字母).
A.a>b>c B.b>c>a C.a=b=c D.无法比较