题目内容
9.已知:①1 mol H2分子中化学键断裂时需要吸收436kJ的能量②1 mol Cl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1 mol HCl分子时释放431kJ的能量
下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
B.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=183kJ/mol
C.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=-183kJ/mol
D.氢气和氯气反应生成1 mol氯化氢气体,反应的△H=-183kJ/mol
C
解析:本题主要考查化学反应中的能量变化情况。书写热化学反应方程式时除标明反应物与生成物的聚集状态外,还必须标明与化学计量数相对应的热量变化值,A不正确;由已知条件知生成2 mol HCl气体时反应物的总键能为:436 kJ+243 kJ=679 kJ,而2 mol HCl的键能为2×431 kJ=862 kJ,所以生成2 mol HCl反应过程中放出的热量为:ΔH=679 kJ·mol-1-862 kJ·mol-1=-183 kJ·mol-1,答案为C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
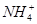 )由大到小的顺序是
)由大到小的顺序是  H++A2-
H++A2-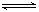 NH4++OH—,要使溶液中c(OH—)/c(NH3·H2O)值增大,可以采取的措施是( )
NH4++OH—,要使溶液中c(OH—)/c(NH3·H2O)值增大,可以采取的措施是( )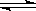 CH3COO-+H+。要使溶液中:
CH3COO-+H+。要使溶液中: