题目内容
将两个铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,称为燃料电池,下列叙述正确的是( )
①通入CH4的电极为正极;②正极的电极反应式是O2+2H2O+4e-=4OH-;③通入CH4的电极反应式是CH4+2O2+4e-=CO2+2H2O;④负极的电极反应式是CH4+10OH--8e-=CO32-+7H2O;⑤放电时溶液中的阳离子向负极移动;⑥放电时溶液中的阴离子向负极移动。
| A.①③⑤ | B.②④⑥ | C.④⑤⑥ | D.①②③ |
B
解析试题分析:①通入CH4的电极为负极。错误;②正极的电极反应式是O2+2H2O+4e-=4OH-,正确;③通入CH4的电极是负极反应式是CH4+10OH--8e-=CO32-+7H2O。错误。④负极的电极反应式是CH4+10OH--8e-=CO32-+7H2O。正确。⑤根据同种电荷互相排斥,异种电荷互相吸引。当放电时溶液中的阳离子向正极移动。错误;⑥放电时溶液中的阴离子向负极移动。正确。
考点:考查燃料电池的电极反应及溶液中离子的移动方向的知识。

 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法错误的是( )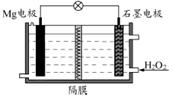
| A.Mg 电极是该电池的负极 |
| B.溶液中Cl-向石墨电极移动 |
| C.该装置中电子从Mg电极流向石墨电极 |
| D.H2O2在石墨电极上发生还原反应 |
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应
Cr2O72–+6Fe2++14H+ 2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是
A.阳极反应为Fe-2e- Fe2+ Fe2+ |
| B.电解过程中溶液pH不会变化 |
| C.反应过程中有Fe(OH)3沉淀生成 |
| D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原 |
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe – 3e– = Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e–= 4OH– |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
下列有关金属腐蚀与防护的说法正确的是( )
| A.生铁比软铁芯(几乎是纯铁)更不容易生锈 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护船壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
某同学设计在KOH溶液中用铂作电极,利用CH3OH和O2的反应来构成原电池。下列说法正确的是( ):①正极上O2得到电子,发生还原反应②每消耗1molCH3OH可以向外电路提供6mole-③该电池的总反应为:2CH3OH+3O2=2CO2+4H2O④电池放电后,溶液的pH不断升高
| A.①② | B.①③ | C.②③ | D.③④ |
有关如下图所示原电池的叙述,正确的是(盐桥中装有含琼脂的KCl饱和溶液) ( )
| A.反应中,盐桥中的K+会移向CuSO4溶液 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.铜片上有气泡逸出 |
| D.反应前后铜片质量不改变 |
下列过程通电后才能进行的是
①电离;②电解;③电镀;④电泳;⑤电化学腐蚀
| A.①②③ | B.①②④ | C.②③④ | D.全部 |
绿色电源“二甲醚-氧气燃料电池”的工作原理如下图所示下列说话正确的是:
| A.氧气应从c处通入,电极Y上发生的反应为O2+4e-+2H2O==4OH- |
| B.电池在放电过程中,电极X周围溶液的pH增大 |
| C.二甲醚应从b处加入,电极X上发生的反应为(CH3)2O—12e-+3H2O=2CO2+12H+ |
| D.当该电池向外电路提供2mol电子时消耗O2约为11.2L |